
(1)某酯的分子式为C6H12O2,其变化如图所示:
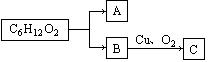
若A能发生银镜反应,C不能发生银镜反应,则该酯的可能结构有 种。
(2)将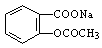 转变为
转变为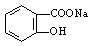 的流程为
的流程为
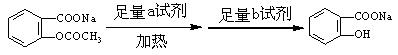
则a试剂是 ,b试剂是 。
【知识点】化学平衡的影响因素、有关反应热的计算、化学电源新型电池、化学平衡的计算
【答案解析】(1)3 (2) NaOH溶液, CO2
解析:(1)酯水解成酸和醇,B能催化氧化,B是醇;A是酸,A能发生银镜反应,所以A是甲
酸,所以酯是甲酸戊酯,同分异构体的数目与戊醇的数目相同,C不能发生银镜反应,则B
中与羟基相连的碳上只有一个氢;即:CH3CH2CH2CH(CH3)-、(CH3CH2)2CH-、(CH3)2CHCH(CH3)- ,
3种。
(3)羧酸钠的官能团不变,所以试剂A为碱:氢氧化钠溶液;水解产物要得到酚羟基,可通
入二氧化碳,不影响羧酸钠原子团;
【思路点拨】本题考查酯的水解及醇的催化氧化,还有羧基、酚羟基的酸性大小,难度中等。


 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化学 来源: 题型:
下列实验操作不正确的是 _。
A.在催化剂存在的条件下, 苯和溴水发生反应可生成无色、比水重的液体溴苯
B.将铜丝弯成螺旋状,在酒精灯上加热变黑后,立即伸入盛有无水乙醇的试管中,完成乙醇氧化为乙醛的实验
C.乙醇中含有少量水可加入生石灰再蒸馏制得无水乙醇
D.试管中先加入一定量浓硫酸,再依次加入适量冰醋酸、无水乙醇,然后加热制取乙酸乙酯
E.实验室制取乙烯时,放入几片碎瓷片,以避免混合液在受热沸腾时剧烈跳动
F.配制银氨溶液时,将稀氨水慢慢滴入硝酸银溶液中,产生沉淀后继续滴加到沉淀刚好溶解为止
G.验证溴乙烷水解产物时,将溴乙烷和氢氧化钠溶液混合,充分振荡溶液、静置、待液体分层后,滴加硝酸银溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中,正确的是( )
A. 久置的氯水与新制的氯水,都能使有色布条褪色
B. 氯气、液氯和氯水是同一种物质
C. 碘化钾溶液中加淀粉溶液变蓝色
D. 加碘盐就是在食盐中加入适量的碘酸钾
查看答案和解析>>
科目:高中化学 来源: 题型:
物A是链状化合物,分子内只含有两种官能团,A和一些化学试剂的反应情况如下图所示:
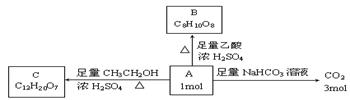
请回答下列问题:
(1)A分子内含有的两种官能团是(写名称) 。
(2)核磁共振氢谱表明A分子中有4个氢处于完全相同的化学环境。则A的结构简式是 。
(3)由A生成B的化学方程式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知有机物A是链状化合物,分子内只含有两种官能团,A和一些化学试剂的反应情况如下图所示:

请回答下列问题:
(1)A分子内含有的两种官能团是(写名称) 。
(2)核磁共振氢谱表明A分子中有4个氢处于完全相同的化学环境。则A的结构简式是 。
(3)由A生成B的化学方程式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
液晶高分子材料应用广泛,新型液晶基元﹣﹣化合物IV的合成线路如下:
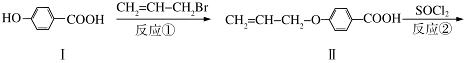
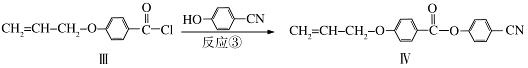
(1)化合物Ⅰ的分子式为 ,1mol化合物Ⅰ最多可与 mol NaOH反应。
(2)CH2=CH﹣CH2Br与NaOH水溶液反应的化学方程式为 (注明条件)。
(3)化合物I的同分异构体中,苯环上一溴代物只有2种且能发生银镜反应的化合物有多种,写出其中一种同分异构体的结构简式 (任写一种)。
(4)反应③的反应类型是 .在一定条件下,化合物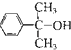 也可与III发生类似反应③的反应生成有机物V,V的结构简式是 。
也可与III发生类似反应③的反应生成有机物V,V的结构简式是 。
(5)下列关于化合物Ⅳ的说法正确的是 (填字母)。
A.属于烯烃 B.能与FeCl3溶液反应显紫色
C.一定条件下能发生加聚反应 D.能使溴的四氯化碳溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是( )
A.臭氧(O3)是一种有鱼腥味、氧化性极强的淡蓝色气体,可用作自来水的消毒剂
B.人造纤维可利用竹子、棉花、麻类的纤维材料制成,而合成纤维是利用自然界的非纤维材料(如石油、煤)通过化学合成方法得到
C.铝及其合金是电气、工业、家庭广泛使用的材料,是因为铝的冶炼方法比较简单
D.有机玻璃是以有机物A(甲基丙烯酸甲酯)为单体,通过加聚反应得到,合成A的一种途经是:CH3C≡CH+CO+CH3OH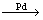
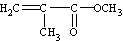 ,其过程符合绿色化学的原则
,其过程符合绿色化学的原则
查看答案和解析>>
科目:高中化学 来源: 题型:
金属铜与金属锰及其化合物在工业上有着广泛的应用:
(1)Cu2+的外围电子排布图可表示为_______________________________________;
(2)Mn基态原子核外处在能量最高的能级上的电子共有________种不同的运动状态;
(3)在铜锰氧化物的催化下,空气中CO被氧化成CO2,HCHO被氧化成CO2和H2O
① N3-和CO2是等电子体,则N3-的结构式为_________________________________;
② HCHO分子中C原子轨道的杂化类型为___________________________________;
(4)向CuSO4溶液中加入过量NaOH溶液可生成[Cu(OH)4]2-。不考虑空间构型,[Cu(OH) 4]2-的结构可用示意图表示为______________________________;
(5) 用晶体的x射线衍射法可以测得阿伏加德罗常数。对金属铜的测定得到以下结果:晶胞为面心立方最密堆积,边长为361pm(提示:3.613=47.05),又知铜的密度为9.00g·cm-3,则铜晶胞的质量是________________________g(保留两位小数);阿伏加德罗常数为_____________________________________(列式计算,保留两位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA表示阿伏加德罗常数,下列说法正确的是
A.1 mol氯气参加氧化还原反应,转移的电子数一定为2NA
B.标准状况下,以任意比混合的氢气和一氧化碳气体共8.96 L,在足量氧气中充分燃烧时消耗氧气的分子数为0.2NA
C.含1 mol FeCl3的溶液中Fe3+的个数为NA
D.1.8g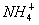 中含有的电子数为0.1NA
中含有的电子数为0.1NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com