
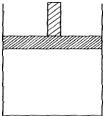
 150��ʱ������ͼ��ʾ���������ܷ�ĸ�������ɻ��������������б��ָ����ϲ�ѹǿ���䣩�м���4L N2��H2�Ļ�����壬�ڴ��������³�ַ�Ӧ������������Բ��ƣ�����Ӧ��ָ���ԭ�¶ȣ�ƽ������������Ϊ3.4L���������������ͬ����������������ܶ�Ϊ5��
150��ʱ������ͼ��ʾ���������ܷ�ĸ�������ɻ��������������б��ָ����ϲ�ѹǿ���䣩�м���4L N2��H2�Ļ�����壬�ڴ��������³�ַ�Ӧ������������Բ��ƣ�����Ӧ��ָ���ԭ�¶ȣ�ƽ������������Ϊ3.4L���������������ͬ����������������ܶ�Ϊ5������ ��1������ʼʱ�������Ϊx L��ƽ������������С��4L-3.4L=0.6L����
N2 ��g��+3H2 ��g��?2NH3��g�� �������V=2
��ʼ��L����x 4-x 0
�仯��L����0.3 0.9 0.6 0.6
ƽ�⣨L����x-0.3 3.1-x 0.6
ƽ��ʱ�������������ͬ����������������ܶ�Ϊ5������Է�������Ϊ5��2=10����$\frac{x-0.3}{3.4}$��28+$\frac{3.1-x}{3.4}$��2=10�����x=1���ݴ˽��
��2���ٳ��백����ƽ�ⲻ�ƶ�ʱ��ƽ����Է�����������ͬ��ͬѹ�£��ܶ�֮�ȵ�������Է�������֮�ȣ��ɣ�1��������֪N2��H2����ʼ���ʵ���֮��Ϊ1��3������ƽ���������г���O��2mol��NH3��ƽ�������ƶ������º�ѹ����ԭƽ��Ϊ��Чƽ�⣬ƽ��ʱ����ֺ������䣻
�ڿ��淴Ӧ����ƽ��ʱ��ͬ�����ʵ�����������ȣ�����ֵ�Ũ�ȡ��������ֲ��䣬�ɴ�����������һЩ�����䣬�ж�ƽ���������Ӧ�淴Ӧ���з����仯�����������ɱ仯�����ٱ仯˵������ƽ�⣻
�۴ӣ�1�������֪��������ת����Ϊ30%�������ֽ���Ϊ70%����0.2mol��70%�����ֽ�����6.44kJ��������2mol�����ֽ���������Ϊ��6.44kJ��$\frac{2mol}{0.14mol}$=92kJ��������2mol�����ų�92kJ������ע�����ʵľۼ�״̬�뷴Ӧ����д�Ȼ�ѧ����ʽ��
��� �⣺��1������ʼʱ�������Ϊx L��ƽ������������С��4L-3.4L=0.6L����
N2 ��g��+3H2 ��g��?2NH3��g�� �������V=2
��ʼ��L����x 4-x 0
�仯��L����0.3 0.9 0.6 0.6
ƽ�⣨L����x-0.3 3.1-x 0.6
ƽ��ʱ�������������ͬ����������������ܶ�Ϊ5������Է�������Ϊ5��2=10����$\frac{x-0.3}{3.4}$��28+$\frac{3.1-x}{3.4}$��2=10�����x=1��
��ӦǰV��N2����V��H2��=1L����4-1��L=1��3����Ӧ�ﵽƽ��ʱV��NH3��=0.6L��N2��ת����Ϊ$\frac{0.3L}{1L}$��100%=30%��
�ʴ�Ϊ��1��3��0.6��30%��
��2�����ټ���0.2m0l���������ڰ���ƽ����Է�������Ϊ17������10���ʻ������ƽ���¶������������������ܶ�����Ӧ�����У�ƽ�������ƶ���������������ƶ����ʻ�������ܶȼ�С���ɣ�1��������֪N2��H2����ʼ���ʵ���֮��Ϊ1��3�����º�ѹ����ԭƽ��Ϊ��Чƽ�⣬ƽ��ʱ����ֺ������䣬ƽ��ʱƽ��Ħ������ԭƽ����ȣ�����������ܶ�Ϊ5��
�ʴ�Ϊ������С��=��
��A��������������緢���Ƚ�����˵����Ӧ�������������䣬��Ӧ����ƽ�⣬��A��ȷ��
B������������������䡢�����ʵ����仯�����������ƽ����Է������������仯����ƽ����Է����������ֲ��䣬˵����Ӧ����ƽ�⣬��B��ȷ��
C��ƽ��ʱ����ֵ����֮������ʼ����ת�����йأ�ƽ��ʱ��һ�����ڻ�ѧ������֮�ȣ���C����
D�����º�ѹ�£��淴Ӧ���������������С����������������ٷ����仯ʱ��˵����Ӧ����ƽ�⣬��D��ȷ��
��ѡ��ABD��
�۴ӣ�1�������֪��������ת����Ϊ30%�������ֽ���Ϊ70%����0.2mol��70%�����ֽ�����6.44kJ��������2mol�����ֽ���������Ϊ��6.44kJ��$\frac{2mol}{0.14mol}$=92kJ��������2mol�����ų�92kJ�������ϳɰ������Ȼ�ѧ����ʽΪ��N2��g��+3H2��g��?2NH3��g����H=-92KJ/mol��
�ʴ�Ϊ��N2��g��+3H2��g��?2NH3��g����H=-92KJ/mol��
���� ���⿼�黯ѧƽ����㡢ƽ��״̬�жϡ��Ȼ�ѧ����ʽ��д�ȣ���2���йؼ��ǶԵ�Чƽ����ɵ����⣬���ؿ���ѧ�����������������ж�ƽ���������Ӧ�淴Ӧ���з����仯�����������ɱ仯�����ٱ仯˵������ƽ�⣮


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na+��Fe2+��NO3-��H+ | B�� | K+��Cu2+��NO3-��H+ | ||
| C�� | H+��Na+��NO3-��HCO3- | D�� | NH4+��Fe2+��NO3-��OH- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
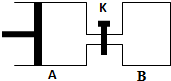 ��ͼ��ʾ������A����ǿ�ƽ���ƶ��Ļ�������A�г���1molX��1molY����B�г���2molX��2molY����ʼʱV��A��=V��B��=aL������ͬ�¶Ⱥ��д������ڵ������£����������Է�����X��g��+Y��g��?Z��g��+2W��g�����ﵽƽ��ʱV��A��=1.2aL���Իش�
��ͼ��ʾ������A����ǿ�ƽ���ƶ��Ļ�������A�г���1molX��1molY����B�г���2molX��2molY����ʼʱV��A��=V��B��=aL������ͬ�¶Ⱥ��д������ڵ������£����������Է�����X��g��+Y��g��?Z��g��+2W��g�����ﵽƽ��ʱV��A��=1.2aL���Իش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ������A��ʾ�ķ�Ӧ����Ϊ0.3 mol/��L•s�� | |
| B�� | ������B��ʾ�ķ�Ӧ����Ϊ0.6 mol/��L•s�� | |
| C�� | 2 sʱ����A��ת����Ϊ70% | |
| D�� | 2 sʱ����B��Ũ��Ϊ0.7 mol•L-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �¶�/�� | 200 | 300 | 400 |
| K | 1.0 | 0.86 | 0.5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | KAl ��SO4��2=K++Al3++2 SO42- | B�� | H2CO3=H++HCO3- | ||
| C�� | Ca��HCO3��2=Ca2++2H++2CO32- | D�� | Ba��OH��2=Ba2++OH2- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ԭ������ | B�� | �������� | C�� | ������� | D�� | Ԫ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com