
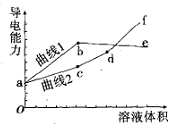
 分别用浓度均为0.5mol/L的NH3•H2O和NaOH溶液,滴定20mL0.01mol/L Al2(SO4)3溶液,随滴定溶液体积的增大,溶液的导电能力变化曲线如图所示,下列说法中正确的是( )
分别用浓度均为0.5mol/L的NH3•H2O和NaOH溶液,滴定20mL0.01mol/L Al2(SO4)3溶液,随滴定溶液体积的增大,溶液的导电能力变化曲线如图所示,下列说法中正确的是( )| A. | 曲线2 代表滴加NH3•H2O溶液的变化曲线 | |
| B. | b和d点对应的溶液均显碱性 | |
| C. | b点溶液中c(NH4+ )>c(SO42- )>c(H+ )>c(OH- ) | |
| D. | df段导电能力升高的原因是发生了反应Al(OH)3+OH-═[Al(OH)4]- |
分析 溶液中离子浓度越大,导电性越强;分别用浓度均为0.5mol/L NH3•H2O和NaOH溶液滴定20 mL 0.01mol/L Al2(SO4)3溶液,一水合氨滴入发生反应:6NH3•H2O+Al2(SO4)3=2Al(OH)3↓+3(NH4)2SO4,氢氧化钠溶液滴入发生的反应为:6NaOH+Al2(SO4)3=2Al(OH)3↓+3Na2SO4 ,Al(OH)3+NaOH═Na[Al(OH)4],所以曲线1为氨水滴入的反应,曲线2位氢氧化钠滴入的反应,据此分析选项.
解答 解:A.一水合氨滴入发生反应:6NH3•H2O+Al2(SO4)3=2Al(OH)3↓+3(NH4)2SO4,氢氧化钠溶液滴入发生的反应为:6NaOH+Al2(SO4)3=2Al(OH)3↓+3Na2SO4 ,Al(OH)3+NaOH=NaAlO2+2H2O,所以曲线1为氨水滴入的反应,曲线2位氢氧化钠滴入的反应,故A错误;
B.b点为硫酸铵溶液,铵根水解溶液显酸性,d点是NaAlO2溶液,偏铝酸根离子水解溶液显碱性,故B错误;
C.b点为硫酸铵溶液,铵根水解溶液显酸性,溶液中离子浓度大小关系为c(NH4+ )>c(SO42- )>c(H+ )>c(OH- ),故C正确;
D.d点是NaAlO2溶液,d点以后氢氧化钠过量,溶液中离子浓度增大,导电性增强,故D错误;
故选C.
点评 本题考查了电解质溶液反应前后溶液导电性的分析判断,主要是离子浓度变化决定溶液导电的变化,注意图象变化的实质理解,题目难度中等,侧重于考查学生的分析能力和应用能力..


 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:选择题
| A. | N2、H2的浓度之比保持不变 | |
| B. | N2和H2的反应速率之比为1:3 | |
| C. | NH3的生成速率与H2的生成速率之比为2:3 | |
| D. | 体系中N2、H2、NH3的分子个数之比为1:3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | V=150 mL | B. | m1=14.6g | ||
| C. | 白色沉淀最大量为15.6g | D. | m2=10.2g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 阳离子 | K+ Mg2+ Fe3+ Al3+ Fe2+ |
| 阴离子 | Cl-CO32- NO3- SO42- SiO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
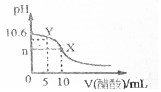 已知常温下CH3COOH和NH3•H2O的电离常数相等,现向10mL浓度为0.01mol•L-1的氨水溶液中滴加相同浓度的CH3COOH溶液,在滴加过程中溶液的pH与所加醋酸的体积关系如图所示.已知100.4=2.5.下列说法错误的是( )
已知常温下CH3COOH和NH3•H2O的电离常数相等,现向10mL浓度为0.01mol•L-1的氨水溶液中滴加相同浓度的CH3COOH溶液,在滴加过程中溶液的pH与所加醋酸的体积关系如图所示.已知100.4=2.5.下列说法错误的是( )| A. | n=7 | |
| B. | 水的电离程度先增大再减小 | |
| C. | 常温下醋酸的电离常数约是1.67×10-5 | |
| D. | Y点溶液中c(NH3•H2O)+c(OH-)=c(CH3COO-)+c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③④ | B. | ①③⑤ | C. | ②④⑤ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 玻璃属于非金属材料,其主要成分是碳酸盐 | |
| B. | 玻璃钢是一种复合材料,由塑料和铁丝复合而成 | |
| C. | 有机物合成材料属于高分子材料,在汽车轮胎、棉花、塑料制品中都存在 | |
| D. | 氮化硅陶瓷是新型无机非金属材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3COO-+H2O?CH3COOH+OH- | B. | HCO3-+H2O?CO32-+H3O+ | ||
| C. | CH3COOH+OH-?CH3COO-+H2O | D. | NaCl+H2O?NaOH+HCl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com