
| A. | H2O(g)═H2(g)+$\frac{1}{2}$O2(g)△H=-485 kJ•mol-1 | B. | H2O(g)═H2(g)+$\frac{1}{2}$O2(g)△H=485 kJ•mol-1 | ||
| C. | 2H2(g)+O2(g)═2H2O(g)△H=485 kJ•mol-1 | D. | 2H2(g)+O2(g)═2H2O(g)△H=-485 kJ•mol-1 |
分析 旧键断裂需要吸收能量,新键的生成会放出能量,反应2H2(g)+O2(g)═2 H2O(g)的△H=反应物的键能和-生成物的键能和=2×436kJ/mol+495kJ/mol-4×463kJ/mol=-485kJ/mol,据此结合热化学方程式的书写原则判断.
解答 解:反应2H2(g)+O2(g)═2 H2O(g)的△H=反应物的键能和-生成物的键能和=2×436kJ/mol+495kJ/mol-4×463kJ/mol=-485kJ/mol,
A.水的分解为吸热反应,该反应的△H>0,正确的热化学方程式为:H2O(g)═H2(g)+$\frac{1}{2}$O2(g)△H=+485 kJ•mol-1,故A错误;
B.水的分解是吸热反应,且反应热与化学计量数成正比,则反应H2O(g)═H2(g)+$\frac{1}{2}$O2(g)的△H=2×463kJ/mol-436kJ/mol-$\frac{1}{2}$×495kJ/mol=+242.5kJ/mol,故B错误;
C.氢气燃烧放热,该反应的△H<0,正确的热化学方程式为:2H2(g)+O2(g)═2H2O(g)△H=-485 kJ•mol-1,故C错误;
D.氢气燃烧放热,反应2H2(g)+O2(g)═2 H2O(g)的△H=2×436kJ/mol+495kJ/mol-4×463kJ/mol=-485kJ/mol,故D正确;
故选D.
点评 本题考查了热化学方程式的书写、反应热的计算,题目难度中等,注意掌握热化学方程式的书写原则,明确化学键与化学反应中能量变化的关系是解题关键,试题培养了学生的分析能力及化学计算能力.


科目:高中化学 来源: 题型:选择题
| A. | Ba(OH)2•8H2O与NH4Cl反应 | B. | H2与Cl2的燃烧反应 | ||
| C. | 铝与稀盐酸反应 | D. | 灼热的碳与CO2反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol | B. | 0.01mol | C. | 6.5g | D. | 5.6g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
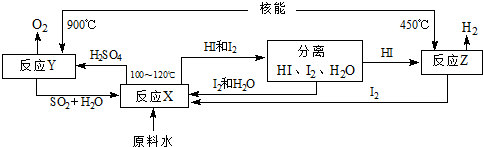
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
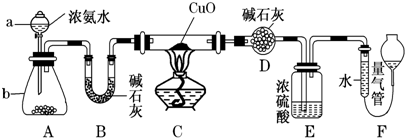
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 ,A与B可形成另一种气态化合物Z,写出实验室制取Z的化学方程式2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O
,A与B可形成另一种气态化合物Z,写出实验室制取Z的化学方程式2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com