

| A. | 供电时的总反应为2H2+O2=2H2O | |
| B. | 负极电极反应为2H2+4OH--4e-=4H2O | |
| C. | 正极电极反应为O2+2H2O+4e-=4OH- | |
| D. | 该燃料电池的能量转化率可达100% |
分析 该燃料电池中,通入燃料氢气的电极是负极、通入氧气的电极是正极,所以a是负极、b是正极,电解质溶液呈碱性,则负极反应式为2H2+4OH--4e-=4H2O、正极电极反应为O2+2H2O+4e-=4OH-,电池反应式为2H2+O2=2H2O,放电过程中,部分化学能转化为热能.
解答 解:A.燃料电池中电池反应式和燃料燃烧方程式相同,所以放电时电池反应式为2H2+O2=2H2O,故A正确;
B.负极上氢气失电子发生氧化反应,和氢氧根离子反应生成水,电极反应式为2H2+4OH--4e-=4H2O,故B正确;
C.正极上氧气得电子发生还原反应,氧气得电子和水反应生成氢氧根离子,电极反应式为O2+2H2O+4e-=4OH-,故C正确;
D.放电过程中,部分化学能转化为热能等,所以该燃料电池的能量转化率不能达到100%,故D错误;
故选D.
点评 本题考查化学电源新型电池,明确原电池原理是解本题关键,难点是电极反应式的书写,要根据电解质溶液酸碱性酸性,注意碱性条件下电极反应式不能生成氢离子,题目难度不大.


 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:高中化学 来源: 题型:解答题
 (1)乙醇的分子结构如图,其中①②③④⑤表示化学键的代号,用代号回答:
(1)乙醇的分子结构如图,其中①②③④⑤表示化学键的代号,用代号回答:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验 | 预期现象和结论 |
在试管加少量的吸收液,再滴加0.01mol•L-1KMnO4溶液 | 若紫红色褪去,证明有SO32-,则说明假设1成立,否则假设1不成立 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Q1=Q | B. | Q1<Q | C. | 2Q1<Q | D. | 无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

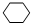
 +Br2→
+Br2→ .
. +2NaOH$→_{△}^{乙醇}$
+2NaOH$→_{△}^{乙醇}$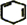 +2NaBr+2H2O.
+2NaBr+2H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2H2(g)+O2(g)=2H2O(l);△H=Q1 2H2(g)+O2(g)=2H2O(g)△H=Q2 | |
| B. | S(g)+O2(g)=SO2(g);△H=Q1 S(s)+O2(g)=SO2(g)△H=Q2 | |
| C. | C(s)+0.5O2(g)=CO(g);△H=Q1 C(s)+O2(g)=CO2(g);△H=Q2 | |
| D. | H2(g)+Cl2(g)=2HCl(g);△H=Q1 0.5H2(g)+0.5 Cl2(g)=HCl(g);△H=Q2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
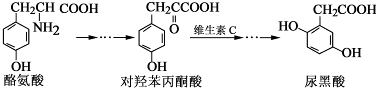
| A. | 对羟基苯丙酮酸分子中在同一平面上的碳原子至少有7个 | |
| B. | 1 mol尿黑酸与足量浓溴水反应,最多消耗3molBr2 | |
| C. | 酪氨酸既能与盐酸反应,又能与氢氧化钠反应 | |
| D. | 1 mol尿黑酸与足量NaHCO3反应,最多消耗3 molNaHCO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com