
下列各组性质的比较中正确的是( )
A. 酸性HClO4<HBrO4<HIO4
B. 碱性Ba(OH)2>Ca(OH)2>Mg(OH)2
C. 稳定性HCl>PH3>H2S
D. 还原性Cl﹣>Br﹣>I﹣
科目:高中化学 来源:2015-2016学年福建省高一下学期期末考试化学试卷(解析版) 题型:选择题
如图是元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是

A. 常压下五种元素的单质中Z单质的沸点最高
B. X元素形成的气态氢化物比W形成的气态氢化物稳定
C. 氯离子的还原性比Y2-元素的简单阴离子的还原性强
D. Y元素的非金属性比W元素的非金属性弱
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高二下学期期末考试化学试卷(解析版) 题型:选择题
下列过程中,一定需要通电才能实现的是
A.电解质电离 B.电化学防腐
C.蓄电池放电 D.电解精炼铜
查看答案和解析>>
科目:高中化学 来源:2015-2016学年重庆四十二中高一下期中化学试卷(解析版) 题型:选择题
应用元素周期律的有关知识,可以预测我们不熟悉的一些元素的单质及其化合物的性质.下列预测中正确的是( )
①Be的氧化物的水化物可能具有两性
②第二周期非金属元素的气态氢化物溶于水后,水溶液均为酸性
③At单质为有色固体,AgAt不溶于水也不溶于稀硝酸
④Li在氧气中剧烈燃烧,产物是Li2O2,其溶液是一种强碱
⑤SrSO4是难溶于水的白色固体
⑥H2Se是无色、有毒、比H2S稳定的气体.
A. ①②③④ B. ②④⑥ C. ①③⑤ D. ②④⑤
查看答案和解析>>
科目:高中化学 来源:2015-2016学年重庆四十二中高一下期中化学试卷(解析版) 题型:选择题
主族元素在周期表中的位置取决于元素原子的( )
A. 原子量和核外电子数
B. 电子层数和最外层电子数
C. 原子量和最外层电子数
D. 电子层数和次外层电子数
查看答案和解析>>
科目:高中化学 来源:2015-2016学年海南省高一下学期期末考试化学试卷(解析版) 题型:推断题
乙烯是重要化工原料,其产量是一个国家石油化工水平的标志。通过石油裂解可以获得乙烯,再以乙烯为原料还可以合成很多的化工产品。已知乙烯能发生以下转化:
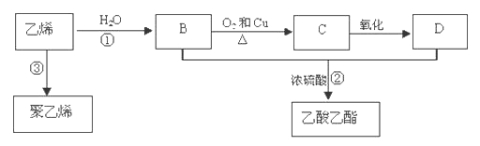
(1)乙烯的结构简式为 。
(2)反应①的反应类型是 ,D中含官能团名称为 。
(3)写出以下反应的化学方程式:[x① ;② ;③ 。
(4)乙烯大量用来生产环氧乙烷,生产工艺主要有两种:
工艺一:
工艺二: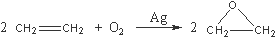
根据绿色化学的原则,理想的生产工艺是原子经济性好的反应,在实际生产中,应采用___________(填“工艺一”或“工艺二”)更环保、更经济。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年海南省高一下学期期末考试化学试卷(解析版) 题型:选择题
欲制取较纯净的1,2 二氯乙烷,可采取的方法是
二氯乙烷,可采取的方法是
A.乙烯与氯化氢加成
B.乙烯与氯气加成
C.乙烷与氯气以1∶2的体积比在光照条件下反应
D.乙烯先与氯化氢加成,再与等物质的量的氯气在光照下反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高一下学期期末考试化学试卷(解析版) 题型:选择题
将等质量的铜片在酒精灯上加热后,分别插入下列溶液中,铜片质量增加的是( )
A.Ca(OH)2溶液 B.稀盐酸 C.硝酸 D.乙醇
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省扬州市高二选修下学期期末调研化学试卷(解析版) 题型:填空题
合成气的主要成分是一氧化碳和氢气,可用于合成二甲醚等清洁燃料。从天然气获得合成气过程中可能发生的反应有:
①CH4(g)+H2O(g) CO(g)+3H2(g) ΔH1=206.1 kJ·mol-1
CO(g)+3H2(g) ΔH1=206.1 kJ·mol-1
②CH4(g)+CO2(g) 2CO(g)+2H2(g) ΔH2=247.3 kJ·mol-1
2CO(g)+2H2(g) ΔH2=247.3 kJ·mol-1
③CO(g)+H2O(g) CO2(g)+H2(g) ΔH3
CO2(g)+H2(g) ΔH3
请回答下列问题:
(1)在一密闭容器中进行反应①,测得CH4的物质的量浓度随反应时间的变化如图1所示。反应进行的前5 min内,v(H2)= ;10 min时,改变的外界条件可能是 。
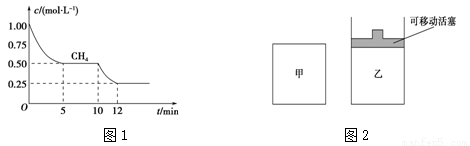
(2)如图2所示,在甲、乙两容器中分别充入等物质的量的CH4和CO2,使甲、乙两容器初始容积相等。在相同温度下发生反应②,并维持反应过程中温度不变。
①可以判断甲容器中反应已达平衡状态的是 。
a.生成CH4的速率是生成CO的速率的2倍
b.容器内压强保持不变
c.容器内气体的密度保持不变
d.容器内各气体的浓度保持不变
②甲乙两容器中反应达到平衡时,下列说法正确的是 。
a.化学反应速率:v (甲)>v (乙)
b.甲烷的转化率:α(甲)<α(乙)
c.压强:P(甲)= P (乙)
(3)反应③中ΔH3= kJ·mol-1。800 ℃时,反应③的化学平衡常数K=1.0,某时刻测得该温度下的密闭容器中各物质的物质的量见下表:
CO | H2O | CO2 | H2 |
0.5 mol | 8.5 mol | 2.0 mol | 2.0 mol |
此时反应③中正、逆反应速率的关系是 (填代号)。
a.v(正)>v(逆) b.v(正)<v(逆) c.v(正)=v(逆) d.无法判断
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com