
把Ca(OH)2放入蒸馏水中,一段时间后达到平衡:
Ca(OH)2(s) Ca2+(aq)+2OH-(aq)。下列说法正确的是( )
Ca2+(aq)+2OH-(aq)。下列说法正确的是( )
A.恒温下向溶液中加入CaO,溶液的pH升高
B.给溶液加热,溶液的pH升高
C.向溶液中加入Na2CO3溶液,其中固体质量增加
D.向溶液中加入少量NaOH固体,Ca(OH)2固体质量不变
科目:高中化学 来源: 题型:
有人用氯化铁、硫酸铜混合溶液进行纸上层析分离实验,实验装置如图所示。
请回答下列问题:
(1)试管中所加展开剂的主要成分是________。
(2)点层析试样是实验的关键操作,进行这一操作时应注意________。
(3)层析操作结束后应进行显色反应,若实验用氨水作为显色试剂,写出本实验中进行显色反应的操作方法:
_____________________________________________。
(4)显色反应后,可观察到________。写出显色反应时所发生反应的离子方程式:_________________________________________________。
(5)若要检验新鲜鸡血中是否含有铁元素,实验操作步骤如下:
①取2 mL新鲜鸡血,将其放入洁净的蒸发皿中,加入2 mL 2 mol·L-1HNO3溶液,加热并不断搅拌。
②将所得溶液蒸干,得到固体粉末。
③取少量固体粉末,将其溶于稀硫酸中,加试剂A,观察现象,判断有无铁元素存在。
操作①的化学原理是________。请列举一种可用于操作③中试剂A的物质________。
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y两种有机物的分子式不同,但均含有C、H或C、H、O,将X、Y以任意比例混合 只要物质的量之和不变,完全燃烧时所消耗的氧气量和生成水的物质的量也分别不变则下列有关判断正确的是: ( )
A、X、Y分子式中氢原子数不一定要相同,碳原子数必定不同
B、若X为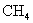 ,则相对分子质量最小的Y是甲醇
,则相对分子质量最小的Y是甲醇
C、若X为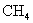 ,则相对分子质量最小的Y是乙二醇
,则相对分子质量最小的Y是乙二醇
D、X、Y的化学式应含有相同的氢原子数,且相差n个碳原子,同时相差2n个氧原子(n为正整数)
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学学习小组为了解硫酸及其盐的某些性质和用途,进行了如下实验探究。
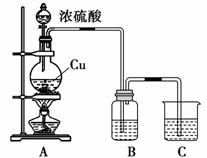
[实验一] 探究浓硫酸的氧化性:
(1)写出烧瓶中反应的化学方程式:____________________________________。
(2)B装置可用于探究SO2的还原性,则B中所用的试剂为:________________(任写一种即可);若B装置是品红溶液,则B中的现象是_______________________________。
[实验二] 检验(NH4)2Fe(SO4)2·6H2O中的金属离子:
(3)请结合化学用语和必要的文字说明如何检验出其中的金属离子(试剂、原理、现象等):______________________________________________________________________。
[实验三] 用KHSO4制取H2O2并测其质量分数:
查阅资料得知:工业上用如下原理制取H2O2:
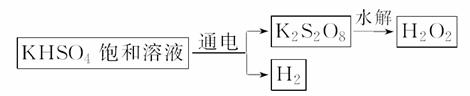
现用此法制取一定浓度的H2O2,并测定H2O2的质量分数。
已知:2MnO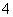 +5H2O2+6H+===2Mn2++8H2O+5O2↑
+5H2O2+6H+===2Mn2++8H2O+5O2↑
①取10.00 mL H2O2溶液(密度为1.00 g·mL-1)置于锥形瓶中加水稀释,并加稀硫酸酸化;
②用0.200 0 mol·L-1KMnO4溶液滴定;
③用同样方法滴定四次,消耗KMnO4溶液的体积分别为:40.00 mL、39.98 mL、42.02 mL、40.02 mL。
(4)用该原理制取H2O2的阳极电极反应式为_______________________________。
(5)进行操作②时,滴入第一滴KMnO4溶液,溶液的紫红色消失很慢,随着滴定的进行,溶液的紫红色消失速率加快,推测其原因可能是_____________________________。
(6)此H2O2溶液中溶质的质量分数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知25℃时,Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17,25 ℃时AgCl固体在下列四个选项中,溶解度最大的是( )
A.100 mL 0.01 mol/L KNO3溶液
B.100 mL 0.01 mol/L 盐酸
C.100 mL 0.01 mol/L AgNO3溶液
D.100 mL 0.01 mol/L KI溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
已知常温下:Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=1.9×10-12,下列叙述正确 的是( )
的是( )
A.AgCl在饱和NaCl溶液中的Ksp和在纯水中的Ksp相同
B.向AgCl的悬浊液中加入NaBr溶液,白色沉淀转化为浅黄色,说明Ksp(AgCl)<Ksp(AgBr)
C.将0.001 mol/L的AgNO3溶液滴入0.001 mol/L的KCl和0.001 mol/L的K2CrO4溶液中先产生Ag2CrO4沉淀
D.向AgCl的悬浊液中滴加浓氨水,沉淀溶解,说明AgCl的溶解平衡向右移动
查看答案和解析>>
科目:高中化学 来源: 题型:
Na、Cu、O、Si、S、Cl是常见的六种元素。
(1)Na位于元素周期表第________周期第________族;S的基态原子核外有________个未成对电子;Si的基态原子核外电子排布式为________________________。
(2)用“>”或“<”填空:
| 第一电离能 | 离子半径 | 熔点 | 酸性 |
| Si____S | O2-____Na+ | NaCl____Si | H2SO4____HClO4 |
(3)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体。在25 ℃、101 kPa下,已知该反应每消耗1 mol CuCl(s),放热44.4 kJ,该反应的热化学方程式是________________________________________________________________________
________________________________________________________________________。
(4)ClO2常用于水的净化,工业上可用Cl2氧化NaClO2溶液制取ClO2。写出该反应的离子方程式,并标出电子转移的方向和数目:________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学兴趣小组的同学们按照下面的实验方法制备氢氧化铁胶体:首先取少量蒸馏水于洁净的烧杯中,用酒精灯加热至沸腾,向烧杯中逐滴滴加饱和的FeCl3溶液继续煮沸,至液体呈透明的红褐色。
FeCl3+3H2O Fe(OH)3(胶体)+3HCl
Fe(OH)3(胶体)+3HCl
(1)判断胶体制备是否成功,可利用胶体的____________________。
(2)在做制备氢氧化铁胶体的实验时,有些同学没有按要求进行,结果没有观察到胶体,请你预测其现象并分析原因:
①甲同学没有选用饱和氯化铁溶液,而是将稀氯化铁溶液滴入沸水中,结果没有观察到________________,其原因是______________________________________________________________。
②乙同学在实验中没有使用蒸馏水,而是用自来水,结果会________________,原因是__________________________________________
____________________________________________________。
③丙同学向沸水中滴加饱和氯化铁溶液后,长时间加热,结果会_______ _________,原因是_________________________________________
_________,原因是_________________________________________
_______________________________________________________。
(3)丁同学按要求制备了Fe(OH)3胶体,但是他又向Fe(OH)3胶体中逐滴加入了稀H2SO4溶液,结果出现了一系列变化。
①先出现红褐色沉淀,原因是___________________________________
________________________________________________________。
②随后沉淀溶解,此反应的离子方程式为_________________________
__________________________ ________________________________。
________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com