
【题目】二甲醚被称为“21世纪的清洁燃料”。利用甲醇脱水可制得二甲醚。反应方程式如下:2CH3OH(g)≒CH3OCH3(g)+H2O(g) ΔH1
(1) 二甲醚亦可通过合成气反应制得,相关热化学方程式如下:2H2(g)+CO(g)≒CH3OH(g) ΔH2
CO(g)+H2O(g)≒CO2(g)+H2(g) ΔH3 3H2(g)+3CO(g)≒CH3OCH3(g) +CO2(g) ΔH4
则ΔH1=__________________(用含有ΔH2、ΔH3、ΔH4的关系式表示).
(2)经查阅资料,上述甲醇脱水反应平衡常数Kp的计算式为lnKp= - 2.205+(2708.6137/T) (Kp为以分压表示的平衡常数,T为热力学温度),且催化剂吸附H2O(g)的量会受压强影响,从而进步影响催化效率。
①在一定温度范围内,随温度升高,CH3OH(g)脱水转化为CH3OCH3(g)的倾向__________ (填“增大”、“不变”或“减小”),ΔH4________2ΔH2+ΔH3 (填“>”、<”或“=”)。
物质 | CH3OH | CH3OCH3 | H2O |
分压/MPa | 0.50 | 0.50 | 0.50 |
②某温度下(此时Kp=100),在密闭容器中加入一定量CH3OH,某时刻测得各组分的压如下:
此时正、逆反应速率的大小:V正____V逆(填“>”、“<”或“=”)。
③200℃时,在密闭容器中加入一定量CH3OH,反应到达平衡状态时,体系中CH3OCH3(g)的物质的量分数为__________(填序号).
A.< 1/3 B.1/3 C.1/3~1/2 D.1/2 E.> 1/2
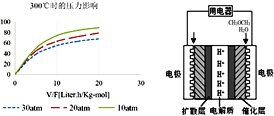
④300℃时,使CH3OH(g)以一定流速通过催化剂,V/F(按原料流率的催化剂量)、压强对甲醇转化率影响如图1所示。请简述在上述条件下,压强对甲醇转化率影响的规律,并解释变化原因__________。
(3)直接二甲醚燃料电池有望大规模商业化应用,工作原理如图2所示。
①负极的电极反应式为__________。
②现利用该电池电解CuC12溶液,当消耗2.3g二甲醚时,电解所得铜的质量为_________g(设电池的能量利用率为50%)。
【答案】ΔH 4-2ΔH2 -ΔH 3 减小 < > C 规律:其他条件不变时,随压强(压力)增大,甲醇转化率降低,原因:压强增大,催化剂吸附水分子的量增多,催化效率降低,相同时间里转化量减少,甲醇转化率降低。 (说明:如规律写错,解释不给分) CH3OCH3—12e-+3H2O=2CO2+12H+ 9.6
【解析】
(1)根据盖斯定律计算;
(2)①lnKp= - 2.205+(2708.6137/T),升高温度lnKp减小,则Kp减小,平衡逆向移动;
②Qp与Kp的关系判断;
③根据lnKp= - 2.205+(2708.6137/T),计算Kp,若催化剂对水蒸气无影响时和催化剂对水蒸气有影响计算P(CH3OCH3)及 CH3OCH3(g)的物质的量分数;
④根据图像可知,温度相同时,随压强的增大,甲醇转化率降低,压强增大,催化剂吸附H2O(g)的量会受压强影响;
(3)①二甲醚燃料电池中,二甲醚失电子,化合价升高,作电池的负极,电解质溶液显酸性,则生成二氧化碳和氢离子;
②根据转移电子数目守恒计算。
(1)①2H2(g)+CO(g)CH3OH(g) ΔH2 ②CO(g)+H2O(g) CO2(g)+H2(g) ΔH3 ③3H2(g)+3CO(g) CH3OCH3(g) +CO2(g) ΔH4,根据盖斯定律,③-②-2①,可得2CH3OH(g) CH3OCH3(g)+H2O(g) ΔH1=ΔH4-2ΔH2 -ΔH 3;
(2)①lnKp= - 2.205+(2708.6137/T),升高温度lnKp减小,则Kp减小,平衡逆向移动,转化成CH3OCH3(g)的倾向减小;ΔH1<0,则ΔH4<2ΔH2 -ΔH 3;
②Qp= ![]() =
=![]() =1<100,平衡正向进行,则V正>V逆;
=1<100,平衡正向进行,则V正>V逆;
③若初始投入的甲醇完全反应时,生成等量的二甲醚和水,二甲醚占据的物质的量分数为![]() ;lnKp= - 2.205+(2708.6137/T),温度为200℃时,Kp=33.78,若催化剂对水蒸气无影响时,且P(CH3OH)=1,则P(CH3OCH3)=5.8,压强之比等于物质的量之比,CH3OCH3(g)的物质的量分数为
;lnKp= - 2.205+(2708.6137/T),温度为200℃时,Kp=33.78,若催化剂对水蒸气无影响时,且P(CH3OH)=1,则P(CH3OCH3)=5.8,压强之比等于物质的量之比,CH3OCH3(g)的物质的量分数为![]() =0.46,答案为C;
=0.46,答案为C;
④根据图像可知,温度相同时,随压强的增大,甲醇转化率降低,压强增大,催化剂吸附H2O(g)的量会受压强影响,导致催化剂吸附水分子的量增多,催化效率降低,相同时间里转化量减少,甲醇转化率降低。
(3)①二甲醚燃料电池中,二甲醚失电子,化合价升高,作电池的负极,电解质溶液显酸性,则生成二氧化碳和氢离子,电极反应式为CH3OCH3-12e-+3H2O=2CO2+12H+;
②消耗2.3g二甲醚时,转移电子的物质的量为0.05×12=0.6mol,铜离子得电子生成单质铜,生成![]() =0.15molCu,即9.6g。
=0.15molCu,即9.6g。


科目:高中化学 来源: 题型:
【题目】有机物A(分子式C6H10O3)是合成某种隐形眼镜材料的单体,A可发生如下变化:
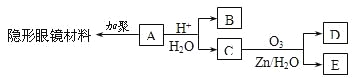
已知:Ⅰ.物质B是最简单的二元醇,可用作汽车发动机抗冻剂;物质D不能发生银镜反应,但能与NaHCO3溶液反应放出气体。
Ⅱ.![]()
回答下列问题:
(1)隐形眼镜材料的结构简式为______________________;
(2)写出物质B在铜催化下与O2反应的化学方程式_____________________;
(3)与C互为同分异构体,分子为链状的酯类物质共有____________种;
(4)请设计合理方案,用物质D制取乙二酸(其他无机原料自选,用反应流程图表示,并注明必要的反应条件)____________;。
例如:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝在酸性或碱性溶液中均可与NO3—发生氧化还原反应,转化关系如下图所示:
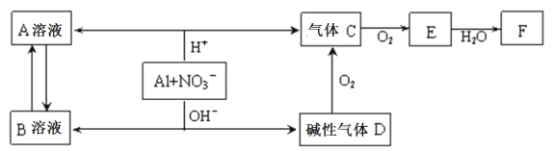
下列说法错误的是
A.B溶液含[Al(OH)4]—
B.A溶液和B溶液混合无明显现象
C.D与F反应生成盐
D.E排入大气中会造成污染
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋是资源的宝库,醢藏着丰富的化学元素,如氯、溴、碘等,海洋资源的综合利用具有非常广阔的前景。
(1)下列说法正确的是_________。
a.AgCl、AgBr、AgI的颜色依次变深 b.F、Cl、Br、I的非金属性依次增强
c.HF、HCl、HBr、HI的还原性的依次增强 d.F2、Cl2、Br2、I2与H2化合由难变易
(2)实验室从海藻灰中提取少量碘的流程如下图:
![]()
①氧化时,可以加入MnO2在酸性条件下进行氧化,反应的离子方程式为:_________。
②上述步骤①②③分离操作分别为过滤、_________、_________。
(3)从海水提取的粗盐中含有Mg2+、Fe2+、Ca2+和SO42—等杂质,“除杂”所需试剂有:①过量的NaOH溶液②过量的Na2CO3溶液③适量的盐酸④过量的BaCl2溶液.试剂的添加顺序为_________。
为使Ca2+完全沉淀,溶液中c(CO32—)应不小于_________mol/L。[已知Ksp(CaCO3)=2.9×10-9,离子浓度小于1×10-5mol/L视为完全沉淀]
(4)目前,利用食盐制取纯碱主要有“氨碱法”和“联合制碱法”两种工艺

①能析出 NaHCO3的原因是_________。
②“氨碱法”是在滤液中加入_________产生NH3,循环使用,但产生大量的度弃物CaCl2;“联合制碱法“是在滤液中继续通入NH3,并加入NaCl粉末以制得更多的副产物_________。
③常温下,向饱和食盐水中通入NH3和CO2,当(HCO3—)=c(NH4+)时,溶液的pH_____7 (填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
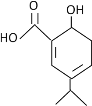
A.如图有机物核磁共振氢谱中出现8组峰
B.如图有机物分子式为C10H12O3
C.分子式为C9H12的芳香烃共有9种
D.蓝烷![]() 的一氯取代物共有6种(不考虑立体异构)
的一氯取代物共有6种(不考虑立体异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】链状高分子化合物![]() 可由有机化工原料
可由有机化工原料![]() 和其他无机试剂通过加成反应、水解反应、氧化反应、缩聚反应制得,则
和其他无机试剂通过加成反应、水解反应、氧化反应、缩聚反应制得,则![]() 是( )
是( )
A.乙醇B.![]() 丁醇C.乙烯D.1,
丁醇C.乙烯D.1,![]() 丁二烯
丁二烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B的结构简式如下
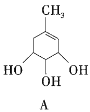
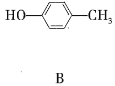
(1)A分子中含有的官能团的名称是__________;B分子中含有的官能团的名称是___________。
(2)A能否与氢氧化钠溶液反应?__________(填“能”或“不能”,下同);B能否与氢氧化钠溶液反应?________。
(3)A在浓硫酸作用下加热可得到B,其反应类型是________________。
(4)A、B各1mol分别加入足量浓溴水,完全反应后消耗单质溴的物质的量分别是______ mol、______mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜元素是一种金属化学元素,也是人体所必须的一种微量元素, 铜也是人类最早发现的金属,是人类广泛使用的一种金属,属于重金属。
(1)写出基态铜原子的价层电子排布式_________________。
(2)简单金属离子在水溶液中的颜色大多与价层电子中含有的未成对电子数有关,如Fe3+呈黄色,Fe2+呈绿色,Cu2+呈蓝色等。预测Cu+为_____色,解释原因________________。
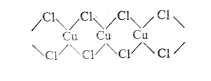
(3)X射线研究证明,CuCl2的结构为链状,如图所示,它含有的化学键类型为_________,在它的水溶液中加入过量氨水,得到 [Cu(NH3)4]Cl2溶液, [Cu(NH3)4]Cl2中H-N-H的夹角_________(填“大于”、“等于”或“小于”)NH3分子中的H-N-H的夹角,原因是___________。
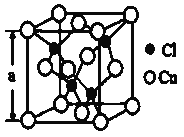
(4)某种铜的氯化物晶体结构如图:此晶体中铜原子的配位数是__________,若氯原子位于铜形成的四面体的体心,且铜原子与铜原子、铜原子与氯原子都是采取最密堆积方式,则氯原子与铜原子半径之比为__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com