
(1)氮和碳的化合物与人类生产、生活密切相关。已知:
N2(g)+O2(g)===2NO(g);ΔH=+180.5 kJ·mol-1
2H2(g)+O2(g)===2H2O(g);ΔH=-483.6 kJ·mol-1
则反应2H2(g)+2NO(g)===2H2O(g)+N2(g);ΔH= 。
(2)在压强为0.1 MPa条件,将a mol CO和3a mol H2的混合气体在催化剂作用下转化为甲醇的反应为CO(g)+2H2(g) CH3OH(g);ΔH<0。
CH3OH(g);ΔH<0。
①该反应的平衡常数表达式为 。
②若容器容积不变,下列措施可增大甲醇产率的是 (填字母)。
A.升高温度
B.将CH3OH从体系中分离
C.充入He,使体系总压强增大
(3)如图所示的装置能吸收和转化NO2和SO2。
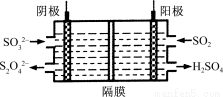
阳极区的电极反应式为 。
②阴极排出的溶液中含S2O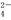 离子,能将NO2气体转化为无污染气体,同时生成的SO
离子,能将NO2气体转化为无污染气体,同时生成的SO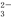 可在阴极区再生。写出该反应的离子方程式: 。
可在阴极区再生。写出该反应的离子方程式: 。
(4)将H2S和空气的混合气体通入FeCl3 、FeCl2 、CuCl2的混合溶液中反应回收S,其物质转化如图所示。
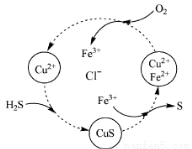
①在图示的转化中,化合价不变的元素是 。
②反应中当有1molH2S转化为硫单质时,保持溶液中Fe3+的物质的量不变,需要消耗O2的物质的量为 。
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案科目:高中化学 来源:2016-2017学年云南省高二上期中化学卷(解析版) 题型:选择题
某学生的实验报告所列出的下列数据中合理的是( )
A.用10mL量筒量取 7.13 mL稀盐酸
B.用托盘天平称量 25.20gNaCl
C.用广泛pH试纸测得某溶液的pH为 2.3
D.用25 mL滴定管做中和滴定时,用去某浓度的碱溶液 21.70 mL
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省高三上模拟一化学试卷(解析版) 题型:选择题
下列说法正确的是
A.一定条件下,使用催化剂能加快反应速率并提高反应物的平衡转化率
B.氨水加水稀释后,溶液中c(NH3·H2O)/c(NH )的值增大
)的值增大
C.需要加热才能发生的反应不一定是吸热反应
D.电解精炼铜时,阴极溶解铜的质量小于阳极析出铜的质量
查看答案和解析>>
科目:高中化学 来源:2017届江西师大附中高三上学期期中化学试卷(解析版) 题型:选择题
氯气溶于水达到平衡后,若其他条件不变,只改变某一条件,下列叙述正确的是( )
A.加入少量水,水的电离平衡向正反应方向移动
B.通入少量SO2,溶液漂白性增强
C.加入少量固体NaOH,一定有c(Na+)=c(Cl-)+c(ClO-)
D.再通入少量氯气, 减小
减小
查看答案和解析>>
科目:高中化学 来源:2017届江西师大附中高三上学期期中化学试卷(解析版) 题型:选择题
LiAlH4是金属储氢材料又是有机合成中的常用试剂,遇水能剧烈反应释放出氢气,LiAlH4在125 ℃时分解为LiH、H2和Al。下列叙 述错误的是( )
述错误的是( )
A.LiAlH4与乙醛作用 生成乙醇,LiAlH4作还原剂
生成乙醇,LiAlH4作还原剂
B.LiAlH4与D2O反应,所得氢气的摩尔质量为4 g·mol-1
C.1 mol LiAlH4在125 ℃时完全分解,转移3 mol电子
D. LiAlH4与水反应生成三种物质时,可能的化学方程式可表示为:
LiAlH4与水反应生成三种物质时,可能的化学方程式可表示为:
LiAlH4+4H2O=Al(OH)3↓+LiOH+4H2↑
查看答案和解析>>
科目:高中化学 来源:2017届江苏省高三上学期期中化学卷(解析版) 题型:选择题
一定条件下进行反应:COCl2(g) Cl2(g)+CO(g)。向2.0 L恒容密闭容器中充入1.0 mol COCl2(g),经过一段时间后达到平衡。反应过程中测得的有关数据见下表:
Cl2(g)+CO(g)。向2.0 L恒容密闭容器中充入1.0 mol COCl2(g),经过一段时间后达到平衡。反应过程中测得的有关数据见下表:
t/s | 0 | 2 | 4 | 6 | 8 |
n(Cl2)/mol | 0 | 0.30 | 0.39 | 0.40 | 0.40 |
下列说法正确的是( )
A.保持其他条件不变,升高温度,平衡时c(Cl2)=0.22 mol·L-1,则反应的ΔH<0
B.若在2 L恒容绝热(与外界没有热量交换)密闭容器进行该反应,化学平衡常数不变
C.保持其他条件不变,起始向容器中充入1.2 mol COCl2、0.60 mol Cl2和0.60 mol CO,反应达到平衡前的速率:v(正)>v(逆)
mol COCl2、0.60 mol Cl2和0.60 mol CO,反应达到平衡前的速率:v(正)>v(逆)
D.保持其他条件不变,起始向容器中充入1.0 mol Cl2和0.8 mol CO,达到平衡时,Cl2的转化率小于60%
查看答案和解析>>
科目:高中化学 来源:2017届江苏省高三上学期期中化学卷(解析版) 题型:选择题
下表所列各 组物质中,物质之间通过一步反应不能实现“甲
组物质中,物质之间通过一步反应不能实现“甲 乙
乙 丙”转化的是( )
丙”转化的是( )
选 | 甲 | 乙 | 丙 |
A | Si | SiO2 | H2SiO3 |
B | NO | NO2 | HNO3 |
C | Na | NaCl | NaOH |
D | CH2=CH2 | CH3CH2OH | CH3CHO |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省娄底市等五校高二上期中化学卷(解析版) 题型:选择题
一定条件下,向密闭恒容容器中加入1.0 mol·L-1X,发生反应:2X(g)  Y(g)+Z(g) △H<0,反应到8min时达到平衡;在14min
Y(g)+Z(g) △H<0,反应到8min时达到平衡;在14min 时改变体系的温度, 16min时建立新平衡。X的物质的量浓度变化如图所示。下列有关说法正确的是
时改变体系的温度, 16min时建立新平衡。X的物质的量浓度变化如图所示。下列有关说法正确的是
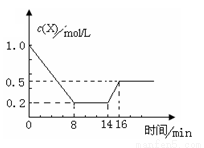
A.0~8min用Y表示该反应速率为0.1mol·L-1·min-1
B.8min时达到平衡,该反应的平衡常数为K= 0.5
C.14min时,改变的反应条是降低了温度
D.16min时的正反应速率比8min时的正反应速率大
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江、吉林两省八校高一上学期期中化学试卷(解析版) 题型:填空题
Ca(ClO)2与浓盐酸反应会生成Cl2,该反应的化学方程式为:
Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O
回答下列问题:
(1)浓盐酸在反应中显示出来的性质是________(填字母)。
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(2)产生0.3 mol Cl2,则转移的电子的物质的量为____________mol。
(3)此反应的离子方程式为_____________________。
(4)用双线桥法标出该反应的电子转移的方向和数目:_________________________。
(5)配平化学方程式:______KMnO4+_______HC1(浓)=_______KCl+_______MnCl2+_______Cl2↑+______H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com