

 +6NaOH$\stackrel{△}{→}$
+6NaOH$\stackrel{△}{→}$ +3NaBr+3H2O;
+3NaBr+3H2O; ;
; (写一种即可).
(写一种即可). 分析 A是芳香烃,根据D的结构简式及转化关系可知A为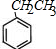 ,乙苯与液溴在催化剂作用下生成B,则B的结构简式为
,乙苯与液溴在催化剂作用下生成B,则B的结构简式为 ;B在氢氧化钠的水溶液中加热发生取代反应生成C,则C为
;B在氢氧化钠的水溶液中加热发生取代反应生成C,则C为 ;C的溶液与二氧化碳气体反应生成D;乙苯在光照条件下与氯气发生取代反应,氯原子取代乙基上的H,由于E为一氯代物,F能够催化氧化生成G,且G的核磁共振氢谱上有4个蜂且峰的面积比为 1:2:2:3,则G只能为
;C的溶液与二氧化碳气体反应生成D;乙苯在光照条件下与氯气发生取代反应,氯原子取代乙基上的H,由于E为一氯代物,F能够催化氧化生成G,且G的核磁共振氢谱上有4个蜂且峰的面积比为 1:2:2:3,则G只能为 ,F为
,F为 、E为
、E为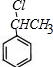 ,据此进行解答.
,据此进行解答.
解答 解:A是芳香烃,根据D的结构简式及转化关系可知A为 ,乙苯与液溴在催化剂作用下生成B,则B的结构简式为
,乙苯与液溴在催化剂作用下生成B,则B的结构简式为 ;B在氢氧化钠的水溶液中加热发生取代反应生成C,则C为
;B在氢氧化钠的水溶液中加热发生取代反应生成C,则C为 ;C的溶液与二氧化碳气体反应生成D;乙苯在光照条件下与氯气发生取代反应,氯原子取代乙基上的H,由于E为一氯代物,F能够催化氧化生成G,且G的核磁共振氢谱上有4个蜂且峰的面积比为 1:2:2:3,则G只能为
;C的溶液与二氧化碳气体反应生成D;乙苯在光照条件下与氯气发生取代反应,氯原子取代乙基上的H,由于E为一氯代物,F能够催化氧化生成G,且G的核磁共振氢谱上有4个蜂且峰的面积比为 1:2:2:3,则G只能为 ,F为
,F为 、E为
、E为 ,
,
(1)根据分析可知,A的结构简式为 ,名称为乙苯;反应Ⅰ为乙苯与液溴反应生成
,名称为乙苯;反应Ⅰ为乙苯与液溴反应生成 ,属于取代反应,
,属于取代反应,
故答案为:乙苯;取代反应;
(2)反应Ⅴ为 转化成
转化成 ,为卤代烃的水解反应,反应条件为氢氧化钠溶液、加热,
,为卤代烃的水解反应,反应条件为氢氧化钠溶液、加热,
故答案为:氢氧化钠溶液、加热;
(3)反应Ⅱ为乙苯邻对位被取代后发生水解反应,反应的化学方程式为: +6NaOH$\stackrel{△}{→}$
+6NaOH$\stackrel{△}{→}$ +3NaBr+3H2O,
+3NaBr+3H2O,
故答案为: +6NaOH$\stackrel{△}{→}$
+6NaOH$\stackrel{△}{→}$ +3NaBr+3H2O;
+3NaBr+3H2O;
(4)根据分析可知,G的结构简式为: ,
,
故答案为: ;
;
(5)F为 ,T是F的同分异构体,它能与氯化铁溶液发生显色反应、苯环上一溴代物有2种,说明F分子中含有酚羟基,且苯环上含有2种H原子,满足条件的有机物如:对乙基苯酚:
,T是F的同分异构体,它能与氯化铁溶液发生显色反应、苯环上一溴代物有2种,说明F分子中含有酚羟基,且苯环上含有2种H原子,满足条件的有机物如:对乙基苯酚: ,
,
故答案为: .
.
点评 本题考查了常见有机物结构与性质,题目难度中等,根据转化关系推断出A的结构简式为解答关键,注意熟练掌握常见有机物结构与性质,试题培养了学生的分析、理解能力及灵活应用能力.


科目:高中化学 来源: 题型:解答题
 钢铁是目前应用最广泛的金属材料,了解钢铁腐蚀的原因与防护方法具有重要意义,对钢铁制品进行防腐处理,可适当延长其使用寿命.
钢铁是目前应用最广泛的金属材料,了解钢铁腐蚀的原因与防护方法具有重要意义,对钢铁制品进行防腐处理,可适当延长其使用寿命.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “洧水”完全燃烧产生的烟可代替松墨用于书写 | |
| B. | “洧水”完全燃烧时热值(单位质量的可燃物燃烧时放出的热量)比甲烷高 | |
| C. | “洧水”的主要成分是煤油 | |
| D. | “洧水”完全燃烧比不完全燃烧的焓变要大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| W | X | |
| Y | Z |
| A. | X元素形成的单核阴离子还原性强于Y | |
| B. | Y元素单质在化学反应中只表现出氧化性 | |
| C. | Z元素氧化物对应水化物的酸性强于Y | |
| D. | X、Y、Z中最简单氢化物稳定性最差的是Y |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③⑤ | B. | ②③④⑥⑦ | C. | ①④⑤ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应中每生成1mol N2O,消耗1.5mol CO | |
| B. | B等物质的量的N2O和CO2含有相等的电子数 | |
| C. | N2O只具有氧化性,无还原性 | |
| D. | 反应中每生成1mol N2O,电子转移的物质的量为3mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子式为C4H10烷烃的二氯取代物 | |
| B. | 分子式为C4H8O2的有机物 | |
| C. | 乙苯的一氯取代物 | |
| D. | 分子式为C3H9N的有机物,其中N原子以三个单键与其他原子相连 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 阳离子 | K+ | Ag+ | Ca2+ | Ba2+ |
| 阴离子 | NO${\;}_{3}^{-}$ | CO${\;}_{3}^{2-}$ | SiO${\;}_{3}^{2-}$ | SO${\;}_{4}^{2-}$ |
| 序号 | 实验内容 | 实验结果 |
| Ⅰ | 向该溶液中加入足量稀盐酸 | 产生白色胶状沉淀并放出标准状况下0.56L气体 |
| Ⅱ | 将Ⅰ的反应混合液过滤,对沉淀洗涤、灼烧至恒重,称量所得固体质量 | 固体质量为2.4g |
| Ⅲ | 向Ⅱ的滤液中滴加BaCl2溶液 | 无明显现象 |
| 阴离子 | NO${\;}_{3}^{-}$ | CO${\;}_{3}^{2-}$ | SiO${\;}_{3}^{2-}$ | SO${\;}_{4}^{2-}$ |
| c/mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 对于反应xA(g)+yB(g)?pC(g)+qD(g).压强与温度对C的质量分数的影响如图所示:
对于反应xA(g)+yB(g)?pC(g)+qD(g).压强与温度对C的质量分数的影响如图所示:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com