
| A. | 2H2(g)+O2(g)$\frac{\underline{\;点燃\;}}{\;}$2H2O(l)△H<0 | B. | 2FeCl3(aq)+Fe(s)═3FeCl2(aq)△H<0 | ||
| C. | CH4(g)+2O2(g)$\frac{\underline{\;点燃\;}}{\;}$CO2(g)+2H2O(l)△H<0 | D. | HNO3(aq)+NaOH(aq)═NaNO3(aq)+H2O(l)△H<0 |
分析 自发的氧化还原反应能设计成原电池,复分解反应不能设计成原电池,根据反应的类型判断.
解答 解:A、2H2(g)+O2(g)$\frac{\underline{\;点燃\;}}{\;}$2H2O(l)△H<0,该反应属于自发的氧化还原反应,所以能设计成原电池,故A不选;
B、2FeCl3+Fe═3FeCl2,该反应属于自发的氧化还原反应,所以能设计成原电池,故B不选;
C、CH4(g)+2O2(g)$\frac{\underline{\;点燃\;}}{\;}$CO2(g)+2H2O(l)△H<0,该反应属于自发的氧化还原反应,所以能设计成原电池,故C不选;
D、HNO3(aq)+NaOH(aq)═NaNO3(aq)+H2O(l)△H<0,该反应属于复分解反应,不是氧化还原反应,所以不能设计成原电池,故D选;
故选D.
点评 本题考查学生设计成原电池的反应应具备的条件,难度不大,根据原电池的构成条件进行设计原电池即可.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | ClO-作氧化剂 | |
| B. | FeO42-为还原产物 | |
| C. | 每产生1 mol FeO42-,转移3 mol电子 | |
| D. | OH-作氧化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②⑤ | C. | ②④ | D. | ③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 标准状况下,铝跟氢氧化钠溶液反应生成1mol氢气时,转移的电子数为2NA | |
| B. | 7 g CnH2n中含有的氢原子数目为NA | |
| C. | 任何气体单质在标况下体积若为22.4L,则含有2NA个原子 | |
| D. | 1mol Na2O2与水反应转移的电子数约为1.204×1024个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.08mol•L-1 | B. | 1.37mol•L-1 | C. | 1.54mol•L-1 | D. | 2.48mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
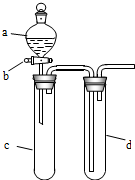 某兴趣小组设计出如图所示装置来改进教材中“铜与硝酸反应”实验,以探究化学实验的绿色化.
某兴趣小组设计出如图所示装置来改进教材中“铜与硝酸反应”实验,以探究化学实验的绿色化.| 方案 | 反应物 |
| 甲 | Cu、浓HNO3 |
| 乙 | Cu、稀HNO3 |
| 丙 | Cu、O2、稀HNO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com