
| A. | 铝热剂 | B. | 水玻璃 | C. | 胆矾 | D. | 漂白粉 |
科目:高中化学 来源: 题型:选择题
| A. | KSCN溶液:酸性KMnO4溶液 | B. | NaOH溶液:Fe粉 | ||
| C. | KSCN溶液:NaOH溶液 | D. | 氨水:NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 反应过程 | 反应现象 | 离子方程式 |
| A | 金属镁与稀盐酸反应 | 有气泡逸出 | Mg+2H++2C-═MgCl2+H2↑ |
| B | 氣化钡溶液与稀硫酸反应 | 有白色沉淀生成 | Ba2++SO42-═BaS04↓ |
| C | 碳酸钠与盐酸反应 | 有气泡逸出 | Na2C03+2H+═CO2↑+H20+ 2Na+ |
| D | 硫酸铜溶液中加入过量的NaOH溶液 | 有白色沉淀产生 | Cu2++20H-═Cu(0H)2↓ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
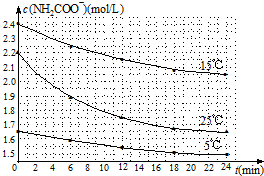
| 温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡气体总浓度 (×10-3mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验目的或结论 |
| A | 向FeCl2溶液中通入Cl2,然后滴加KSCN溶液 | 验证Cl2的氧化性比Fe3+强 |
| B | 向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀生成 | 该溶液中不一定含有SO42- |
| C | 用洁净的玻璃棒蘸取某溶液进行焰色反应,火焰呈黄色 | 该溶液中一定含有Na+,一定无K+ |
| D | 将某气体通入品红溶液中,溶液褪色 | 该气体中一定含有SO2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO2溶于水:3NO2+H2O=2H++2NO3-+NO | |
| B. | 用惰性电极电解CuSO4溶液:2Cu2++2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu↓+4H++O2↑ | |
| C. | NaClO溶液中通入过量的SO2:ClO-+SO2+H2O=HClO+HSO3- | |
| D. | NaAlO2溶液中通入过量的CO2:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
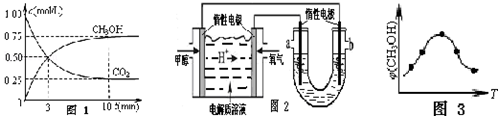
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH固体 | B. | CH3COONa固体 | C. | NaCl固体 | D. | CuCl2固体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com