
ÓĆCl2Éś²śÄ³Š©ŗ¬ĀČÓŠ»śĪļŹ±»į²śÉśø±²śĪļHC1”£ĄūÓĆ ·“Ó¦A£¬æÉŹµĻÖĀȵÄŃ»·ĄūÓĆ”£
·“Ó¦A£¬æÉŹµĻÖĀȵÄŃ»·ĄūÓĆ”£
·“Ó¦A£ŗ4HCl£«O22Cl2£«2H2O
£Ø1£©ŅŃÖŖ:¢ń”¢·“Ó¦AÖŠ£¬ 4mol HCl±»Ńõ»Æ£¬·Å³ö115.6kJµÄČČĮ攣
4mol HCl±»Ńõ»Æ£¬·Å³ö115.6kJµÄČČĮ攣
¢ņ”¢
¢Ł·“Ó¦AµÄČČ»Æѧ·½³ĢŹ½ŹĒ________________________”£
¢Ś¶ĻæŖ1 mol H”ŖO ¼üÓė¶ĻæŖ 1 mol H”ŖCl ¼üĖłŠčÄÜĮæĻą²īŌ¼ĪŖ__________kJ£¬H2OÖŠH”Ŗ0 ¼ü±ČHClÖŠH”ŖCl¼ü£ØĢī”°Ēæ”±»ņ”°Čõ”±£©_______________”£
£Ø2£©ŗĻ³É°±¹¤³§³£Ķعż²ā¶Ø·“Ó¦Ē°ŗó»ģŗĻĘųĢåµÄĆܶȥ“Č·¶Ø°±µÄ×Ŗ»ÆĀŹ”£Ä³¹¤³§²āµĆŗĻ³ÉĖžÖŠN2”¢H2»ģŗĻĘųĢåµÄĆܶČĪŖ0.5536g/L£Ø±ź×¼×“æö£©£¬“ÓŗĻ³ÉĖžÖŠ³öĄ“µÄ»ģŗĻĘųĢåŌŚĻąĶ¬Ģõ¼žĻĀĆܶČĪŖ0.693g/L£Ø±ź×¼×“æö£©”£øĆŗĻ³É°±³§N2µÄ×Ŗ»ÆĀŹĪŖ___________”£
 µ¼Ń§Č«³ĢĮ·““ÓÅѵĮ·ĻµĮŠ“š°ø
µ¼Ń§Č«³ĢĮ·““ÓÅѵĮ·ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŌŚŗ¬ÓŠNA øöCH3COO-µÄ“×ĖįČÜŅŗÖŠ£¬H+ŹżÄæĀŌ“óÓŚNA | |
| B£® | ³£ĪĀĻĀ£¬5.6 L NOŗĶ5.6 L O2µÄ»ģŗĻĘųĢåÖŠŗ¬ÓŠµÄ·Ö×ÓŹżĪŖ0.5NA | |
| C£® | 16.9 g BaO2¹ĢĢåÖŠŅõ”¢ŃōĄė×Ó×ÜŹżĪŖ0.3NA | |
| D£® | ŗ¬ÓŠ1 mol Fe£ØOH£©3µÄĒāŃõ»ÆĢś½ŗĢåÖŠŗ¬ÓŠ½ŗĮ£ŹżĪŖNA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
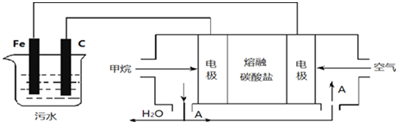
 ĒāŃõ»Æ¼ŲŹĒÖŲŅŖµÄ¹¤Ņµ²śĘ·£®¹¤ŅµĘ·ĒāŃõ»Æ¼ŲµÄČÜŅŗÖŠŗ¬ÓŠÄ³Š©ŗ¬ŃõĖįøłŌÓÖŹ£¬æÉÓĆĄė×Ó½»»»Ä¤·Øµē½āĢį“森µē½ā²ŪČװӊŃōĄė×Ó½»»»Ä¤£ØÖ»ŌŹŠķŃōĄė×ÓĶعż£©£¬Ę乤×÷ŌĄķČēĶ¼ĖłŹ¾£®Ēė»Ų“š£ŗ
ĒāŃõ»Æ¼ŲŹĒÖŲŅŖµÄ¹¤Ņµ²śĘ·£®¹¤ŅµĘ·ĒāŃõ»Æ¼ŲµÄČÜŅŗÖŠŗ¬ÓŠÄ³Š©ŗ¬ŃõĖįøłŌÓÖŹ£¬æÉÓĆĄė×Ó½»»»Ä¤·Øµē½āĢį“森µē½ā²ŪČװӊŃōĄė×Ó½»»»Ä¤£ØÖ»ŌŹŠķŃōĄė×ÓĶعż£©£¬Ę乤×÷ŌĄķČēĶ¼ĖłŹ¾£®Ēė»Ų“š£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| Ėį | µēĄėĘ½ŗā³£ŹżK |
| CH3COOH | 1.76”Į10-5 |
| H2CO3 | K1=4.3”Į10-7 K2=5.61”Į10-11 |
| H3PO4 | K1=7.52”Į10-3 K2=6.23”Į10-8 K3=2.20”Į10-13 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
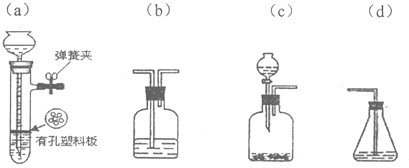
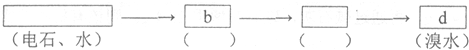
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÉĻŹöø÷·“Ó¦¾ł¼ČŹōÓŚŃõ»Æ»¹Ō·“Ó¦£¬ÓŠŹōÓŚĄė×Ó·“Ó¦ | |
| B£® | Ńõ»ÆŠŌ£ŗKMnO4£¾K2Cr2O7£¾Cl2£¾MnO2 | |
| C£® | ŃĪĖįµÄÅضČŌ½“ó£¬Cl-µÄ»¹ŌŠŌŌ½Ēæ | |
| D£® | ĆæÉś³É1molCl2£¬ÉĻŹöø÷·“Ó¦×ŖŅʵĵē×ÓŹż¾łĪŖ2NA£ØNAĪŖ°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com