
����Ŀ����1����̬��ԭ�ӵļ۵����Ų�ͼΪ
��2����֪TiCl4��ͨ�����������ɫҺ�壬�۵�Ϊ��37�� ���е�Ϊ136�� ����֪TiCl4Ϊ ���壮
��3���������Ѿ�����������Ϊ��״�ۺ���ʽ�����ӣ��ṹ��ͼ��ʾ����������Ti��O��ԭ����֮��Ϊ ��
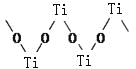
��4��Co��һ��������ľ�����ͼ��ʾ���ڸþ�������һ����ԭ�ӵȾ������������ԭ���� �����������Ͽ�ѧ����ʵ����һ������С�鷢������5K�³��ֳ����Եľ��壬�þ������CoO2�IJ�״�ṹ����ͼ��ʾ��С���ʾCoԭ�ӣ������ʾOԭ�ӣ��������ô��������ظ��ṹ��Ԫʾ��ͼ��������CoO2�Ļ�ѧ����� ��


��5����C��Mg��Ni����Ԫ����ɵ�һ�ּ������ṹ�Ļ�������г����ԣ��侧����Cλ������λ�ã�Mgλ�ڶ��ǣ�Niռ������λ�ã��û�����Ļ�ѧʽΪ ��������Mgԭ����Χ���������Niԭ���� ���������ͳ������Ͼ�������a=0.38nm������þ�����ܶ� ��gcm��3����������λ��Ч���֣�
��6�������Ѿ����ṹ��ͼ��ʾ������ԭ�ӵİ뾶Ϊr����þ�������ı���ʽΪ

���𰸡���1��![]()
��2�����Ӿ���
��3��1��1��
��4��12��D
��5��MgNi3C�� 12��6.45gcm-3��2�֣�
��6��8 r3��2�֣�
�������������������1��Tiԭ�Ӽ۵���Ϊ3d��4s���ӣ�3d�ܼ�����2�����ӡ�4s�ܼ�����2�����ӣ���۵����Ų�ͼΪ![]() ��
��
�ʴ�Ϊ��![]() ��
��
��2�����Ӿ����۷е�ϵͣ��������۷е�ϵͣ����ڷ��Ӿ��塣
�ʴ�Ϊ�����ӣ�
��3��ÿ��Oԭ�ӱ�����Tiԭ�ӹ��á�ÿ��Tiԭ�ӱ�����Oԭ�ӹ��ã����þ�̯���������ԭ�Ӹ���֮��Ϊ1��1��
�ʴ�Ϊ��1��1��
��4���������ᄃ���ṹ��֪������Co��Oԭ����Ŀ֮��Ϊ1��1�������ɫ��ΪCoԭ�ӣ��Զ���Coԭ��Ϊ�о�������֮�Ⱦ������������ԭ��λ�����ģ�ÿ������Ϊ8���������ã�ÿ������Ϊ2���������ã��ڸþ�������һ����ԭ�ӵȾ������������ԭ����ĿΪ![]() =12��
=12��
CoO2���ظ��ṹ��Ԫʾ��ͼ��Co��Oԭ����Ŀ֮��ӦΪ1��2����ͼ���֪��A��Co��Oԭ����Ŀ֮��Ϊ1��4��![]() =1��2�����ϣ�B��Co��Oԭ����Ŀ֮��Ϊ��1+4��
=1��2�����ϣ�B��Co��Oԭ����Ŀ֮��Ϊ��1+4��![]() ����4=1��2�����ϣ�C��Co��Oԭ����Ŀ֮��Ϊ4��
����4=1��2�����ϣ�C��Co��Oԭ����Ŀ֮��Ϊ4��![]() ��4��
��4��![]() =1��2�����ϣ�D��Co��Oԭ����Ŀ֮��Ϊ1��4��
=1��2�����ϣ�D��Co��Oԭ����Ŀ֮��Ϊ1��4��![]() =1��1�������ϡ�
=1��1�������ϡ�
�ʴ�Ϊ��12��D��
��5��������̼λ�����ģ�ֻ��1����þλ�ڽ��ϣ�ÿ��þԭ�ӱ�8���������ã���ÿ��������þԭ�Ӹ���Ϊ8��![]() =1������λ�����ģ�ÿ����ԭ�ӱ������������ã���ÿ����������ԭ�Ӹ���Ϊ6��
=1������λ�����ģ�ÿ����ԭ�ӱ������������ã���ÿ����������ԭ�Ӹ���Ϊ6��![]() =3�����ʾ��廯ѧʽΪMgNi3C��ÿ��������þ��Χ��3����ԭ�ӣ�ÿ��þ���˸��������ã��Ϸ����ĸ���������������ԭ�ӣ��ԳƵ��·�Ҳ��������һ��12����
=3�����ʾ��廯ѧʽΪMgNi3C��ÿ��������þ��Χ��3����ԭ�ӣ�ÿ��þ���˸��������ã��Ϸ����ĸ���������������ԭ�ӣ��ԳƵ��·�Ҳ��������һ��12����
������ܶȣ���=![]() ��
��
�ʴ�Ϊ��MgNi3C��12��6.45gcm-3��
��6�������Ѿ����ṹ��ͼ��ʾ������ԭ�ӵİ뾶Ϊr����þ����߳�ԼΪ2r������������ı���ʽΪ(2r)3=8r3��
�ʴ�Ϊ��8r3��


 53���ò�ϵ�д�
53���ò�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ܱ������г�������A��B��������ӦaA(g)��bB(g)![]() cC(g)����Ӧ�����У�����A�����������C������������¶�(T)�ı仯������ͼ��ʾ������˵����ȷ����(����)
cC(g)����Ӧ�����У�����A�����������C������������¶�(T)�ı仯������ͼ��ʾ������˵����ȷ����(����)

A. �÷�Ӧ��T1��T3�¶�ʱ�ﵽ��ѧƽ��
B. �÷�Ӧ��T2�¶�ʱ�ﵽ��ѧƽ��
C. �÷�Ӧ���淴Ӧ�Ƿ��ȷ�Ӧ
D. �����¶ȣ�ƽ���������Ӧ�����ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�ָ�Ч�Ͷ���ũҩ��ɱ��������ĺϳ�·�����£�
�ϳ�1��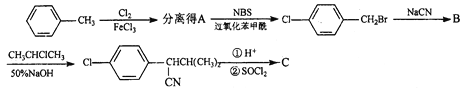
�ϳ�2��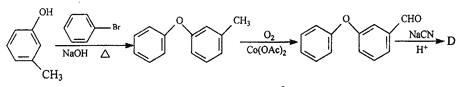
�ϳ�3��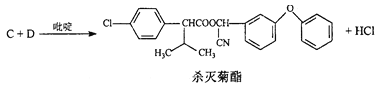
��1��![]() �еĹ�������____________________________(������)��
�еĹ�������____________________________(������)��
��2��C�Ľṹ��ʽΪ_____________���ϳ�3�е��л���Ӧ����Ϊ______________��
��3���ںϳ�2�У���һ���͵ڶ�����˳���ܵߵ���������______________��
��4��д����������������D��ͬ���칹��Ľṹ��ʽ______________��
������2������ ����������4�ֲ�ͬ��ѧ�������� ���ܷ���ˮ�ⷴӦ
��5����֪��![]()
�л���E(![]() )�Ǻϳ�һ�ֿ�����ҩ����Ҫ�м��塣��������֪ʶ����������Ϣ��д����CH3Br��Ϊ�л�ԭ��(���Լ��ͷ�Ӧ������ѡ)�ϳ�E��·������ͼ���ϳ�·������ͼʾ�����£�
)�Ǻϳ�һ�ֿ�����ҩ����Ҫ�м��塣��������֪ʶ����������Ϣ��д����CH3Br��Ϊ�л�ԭ��(���Լ��ͷ�Ӧ������ѡ)�ϳ�E��·������ͼ���ϳ�·������ͼʾ�����£�![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������a mol/L ��NaX��b mol/L��NaY��������Һ������˵����ȷ����
A. ��a=b��c(X��)= c(Y��)+ c(HY)����HXΪǿ��
B. ��a=b��pH(NaX)>pH(NaY),��c(X��)+ c(OH��)> c(Y��)+ c(OH��)
C. ��a>b��c(X��)= c(Y��)��������HX>HY
D. ������Һ�������ϣ���c(Na+)="(a+b)" mol/L(���Ի�Ϲ����е�����仯)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͨ������ȼ�ϵ������ʽ�ͼ�ʽ���֣��Իش��������⣺
��1������ʽ�����У�������Ӧ������Ϊ ��������Ӧ������Ϊ ����ʽ��صĵ缫��Ӧ��
������ �������� ��
�������ҺpH�ı仯 �����������������С����������������
��2���ڼ�ʽ�����У���ʽ��صĵ缫��Ӧ��
������ �������� ��
�������ҺpH�ı仯 �����������������С����������������
��3������ȼ�ϵ��������Ϊ�Ϻ������еĽ�ͨ����֮һ�������й�˵������ȷ����________��
A��̫������ֽ�ˮ�������ȵ��ˮ��������Ϊ��ѧ
B������ȼ�ϵ����Ϊ�����������ܱ�������
C����ϡH2SO4��KOHΪ���ʵ�����ȼ�ϵ�صĸ����缫��Ӧʽ��ͬ
D����ϡH2SO4��KOHΪ���ʵ�����ȼ�ϵ�ص��ܷ�Ӧʽ��ͬ
��4�����綯�������˸�Ч���õ�һ�����Ϳɳ���أ��õ�ص��ܷ�ӦʽΪ��3Zn��2K2FeO4��8H2O![]() 3Zn(OH)2��2Fe(OH)3��4KOH��
3Zn(OH)2��2Fe(OH)3��4KOH��
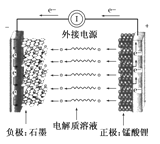
���õ�طŵ�ʱ������ӦʽΪ_________________��
���ŵ�ʱÿת��3 mol���ӣ�������________ mol K2FeO4����ԭ��
��������ӵ���ڻ�϶������ȴ�������Ӧ������ռ��������λ��
��ط�ӦʽΪ��Li1��xMnO4��Lix ![]() LiMnO4�������й�˵������ȷ����________��
LiMnO4�������й�˵������ȷ����________��
A���ŵ�ʱ��ص�������ӦʽΪ��Li1��xMnO4��xLi����xe��===LiMnO4
B���ŵ�����У�ʯīû�е�ʧ����
C���õ��Ҳ����KOH��Һ�Ļ�������������
D�����ʱ����ϱ����������ĵ缫Ӧ����ӵ�Դ�ĸ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������A��B��C��D��E��F���ֶ�����Ԫ��,�����ڻ�ѧ��Ӧ�о����γɼ������ӻ�������,��A��B��C��D���Ӿ�����ͬ�ĵ��Ӳ�ṹ����֪��
1.������F�ĵ�����һ����ɫ����,������ɱ����������
2.A�������������������������Һ,�����������
3.C���⻯�����G�Ǿ���10���ӵ���,�ҿ��Է�������ת����
![]()
4.E��D��ͬ����Ԫ��,�⻯�H2E��������Ϊ��̬��
5.B��D���γ���������Ϊ1��1��2��1�����ӻ�����X��Y��
��ش��������⣺
��1��д��CԪ��λ�����ڱ��е�λ��________��
��2��AԪ�ص�ԭ�ӽṹʾ��ͼΪ________��
��3��B��C��D����Ԫ���γɵĻ�������������ѧ��������________��
��4���ǽ����ԣ�E_____������ڻ�С�ڣ�F��������ʵ����˵����________�����û�ѧ����ʽ��ʾ��
��5��B2E�ĵ���ʽΪ_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ij��ѧ��ȤС���ͬѧѧϰԪ��������ʱ��Ƶ�����ʵ�鷽����
��ʵ��һ��ʵ�鲽�����£�
ʵ����� | ʵ�鲽�� |
�� | �����Ƶ�Na2S��Һ�еμ����Ƶ���ˮ |
�� | ��þ��Ͷ��1mol/L��ϡ������ |
�� | ������Ͷ��1mol/L��ϡ������ |
��1����Ƹ�ʵ�鷽����Ŀ���ǣ�̽��ͬ����Ԫ�ص�__________________________��
��2��ʵ��ٵ������� ����Ӧ�Ļ�ѧ����ʽ�� ��
��ʵ����� Ϊ��֤Cl2��Br2�ķǽ�����ǿ�������������ʵ�飺(�ɹ�ѡ����Լ��У���ˮ����ˮ��NaCl��Һ��NaBr��Һ���ƾ������Ȼ�̼)ʵ�鲽������ͼ��
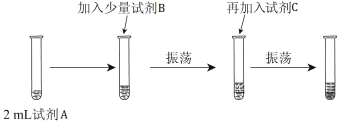
��3���Լ�A�� ���Լ�B�� ���Լ�C�� ��
��4���Լ�C��ʵ��������������� ������C�����ú��������ǣ� �����Ϸ�Ӧ����֤��Cl2�ķǽ�����_______(�ǿ�ڡ������ڡ�)Br2�ķǽ����ԣ���Ӧ�����ӷ���ʽΪ��_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ������ҵ��һ��������з�Ӧ�ϳɼ״�CO(g)+2H2 (g)![]() CH3OH(g) ��H
CH3OH(g) ��H
��1���±����������Ƿ�Ӧ�ڲ�ͬ�¶��µĻ�ѧƽ�ⳣ��(K)��
![]()
�ɱ��������жϦ�H________0 (�����������������)����ѧƽ�ⳣ������ʽK=________��
��2��300��ʱ�������Ϊ2.0 L���ܱ�������ͨ��2 mol CO��4 mol H2������20 s�ﵽƽ��״̬��
������20 s��CO�ķ�Ӧ����Ϊ________����ʱ�����м״����������Ϊ_________��
����������ƽ����ϵ��ͬʱ����1mol CO��2mol H2��1mol CH3OH���壬ƽ���ƶ������__________(����ҡ����������ƶ���)��ԭ����________________________
��3����֪�ڳ��³�ѹ�£�
��2CH3OH(l)��3O2 (g) = 2CO2 (g)��4H2O(g) ��H����1277.0kJ/mol
��2CO(g)+O2 (g) = 2CO2(g) ��H����566.0kJ/mol
��H2O(g) =H2O(l) ��H����44kJ/molд���״�����ȫȼ������һ����̼��Һ̬ˮ���Ȼ�ѧ����ʽ��
__________________��
��4���״�������������ȼ�ϵ�أ�д������������Ϊ����ʼ״�ȼ�ϵ�ظ�����Ӧʽ_______________����ͼ�����KI��Һ�Ƶ⣬�ڴ��Թ��м��뱥�͵�KI��Һ��Ȼ���ټ��뱽������һ��ʯī�缫��һ�����缫��ʹ�ø�ȼ�ϵ������Դ�����缫�뼫___________�������������ӣ�ͨ��һ��ʱ��Ͽ���Դ�����Թܣ��ϲ���ҺΪ_______ɫ������ 1.27g�ⵥ������ʱ,��Ҫ_______g CH3OH��
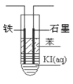
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��2,6��������4���һ�����Ľṹ��ʽ��______________________����һ�ȴ�����_________�֡�
��2����ϵͳ�����������л���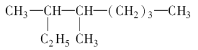 ��������______________��
��������______________��
��3��ij������ķ���ʽΪC5H11Cl����˴Ź�������ͼ����ʾ���ַ������֮��Ϊ6:4:1���������ʵĽṹ��ʽΪ______ _��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com