
下列离子方程式或化学反应方程式与所述事实相符且正确的是
A.将少量SO2气体通入NaClO溶液中:SO2+H2O+2ClO-=SO32-+2HClO
B.将2molSO3气体通入一密闭容器中,达平衡后吸收QkJ热量,则该反应的热化学方程式为:2SO3(g)  2SO2(g)+O2(g) △H=+Q kJ/mol
2SO2(g)+O2(g) △H=+Q kJ/mol
C.向含有0.4 mol FeBr2的溶液中通入0.3 mol Cl2充分反应:
4Fe2++2Br-+3Cl2=4Fe3++6Cl-+Br2
D.NH4Al(SO4)2溶液中加入Ba(OH)2溶液使SO42-完全沉淀:
Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O
 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案科目:高中化学 来源: 题型:
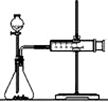
在如图所示的原电池中,下列说法正确的是
A.负极发生还原反应
B.正极反应为 Cu-2e-===Cu2+
C.电子由铜片通过导线流向锌片
D.反应一段时间后,溶液的酸性减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究。
实验一:他们利用Cu、Fe、Mg和不同浓度的硫酸(0.5 mol/L、2 mol/L、18.4 mol/L),设计实验方案来研究影响反应速率的因素。甲同学研究的实验报告如下表:
| 实验步骤 | 现象 | 结论 |
| ①分别取等体积的2 mol/L硫酸于试管中; ②分别投入大小、形状相同的Cu、Fe、Mg。 | 反应快慢: Mg>Fe>Cu | 反应物的性质越活泼,反应速率越快。 |
 (1)甲同学的实验目的是__________________________________________;要得出正确的实验结论,还需控制的主要实验条件是___________________________________。
(1)甲同学的实验目的是__________________________________________;要得出正确的实验结论,还需控制的主要实验条件是___________________________________。
(2)乙同学为了更精确地研究浓度对反应速率的影响,利用右图装置进行定量实验。完成该实验应选用的实验药品是______________________
_____________;应该测定的实验数据是_____________________________。
实验二:某同学发现,纯度、质量、表面积都相同的两铝片与H+浓度相同的盐酸和硫酸在同温同压下反应时产生氢气的速率差别很大,铝和盐酸反应速率更快。他决定对其原因进行探究。填写下列空白:
①该同学认为:由于预先控制了反应的其他条件,那么,两次实验时反应的速率不一样的原因,只有以下五种可能:
原因Ⅰ:Cl-对反应具有促进作用,而SO42-对反应没有影响;
原因Ⅱ:____________________________________________________________________;
原因Ⅲ:Cl-对反应具有促进作用,而SO42-对反应具有阻碍作用;
原因Ⅳ:Cl-、SO42-均对反应具有促进作用,但Cl-影响更大;
原因Ⅴ:____________________________________________________________________。
②该同学设计并进行了两组实验,即得出了正确结论。他取了两片纯度、质量、表面积均相同、表面经过砂纸充分打磨的铝片,分别放入到盛有同体积、c(H+)相同的稀硫酸和盐酸的试管(两试管的规格相同)中。
a.在盛有硫酸的试管中加入少量NaCl或KCl固体,观察反应速率是否变化。
b.在盛有盐酸的试管中加入少量Na2SO4或K2SO4固体,观察反应速率是否变化。
若观察到实验a中______________________,实验b中________________________,则说明
原因Ⅲ是正确的。依次类推。该同学通过分析实验现象,得出了结论:Cl-对反应具有加速作用。
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA表示阿伏加德罗常数的值,下列叙述中正确的是
A.常温常压下,48gO3与O2混合气体中含氧原子数为3NA
B.1.8g的NH4+离子中含有的电子数为0.1NA
C.11.2L氧气中所含有的原子数为NA
D.标准状况下,22.4 LC6H14中所含碳原子数分子数为6NA
查看答案和解析>>
科目:高中化学 来源: 题型:
化学和环境保护、食品营养、材料应用等密切相关。
(1)(3分)防治环境污染、改善生态环境已成为全人类的共识。
①下列各项中,完成空气质量报告时不需要监测的是 (填字母)。
a.二氧化碳的浓度
b.二氧化硫的浓度
c.可吸入颗粒物的浓度
②下列做法中不利于改善环境质量的是 (填字母)。
a.将废旧电池进行深埋处理
b.充分利用风能等新能源
c.给汽车加装尾气催化净化装置
③工业废水需处理达标后才能排放。轧钢厂排出的废水主要是含盐酸的酸性废水,处理此废水可采用的方法是 (填字母)。
a.氧化还原法 b.中和法 c.沉淀法
(2)(5分)营养平衡、合理用药是保证人体健康和生活质量的重要途径。
①人体需要的营养素主要有糖类、油脂、 、无机盐、维生素和水。在氢、钠、铁这三种元素中,属于人体生命活动必需微量元素的是 。(填元素符号)
②下列物质中,具有抗菌消炎疗效的是 (填字母)。
a.氨基酸 b.阿斯匹林 c.青霉素
③有些药片常用淀粉作为黏合剂,淀粉进入人体后在人体内酶的催化作用下逐步水解,最终转化为 (填物质的名称)。维生素C能防治坏血病并具有还原性,验证维生素C有还原性可以使用淀粉溶液和 试剂共同完成。
(3)(7分)材料是人类社会发展的物质基础,材料科学的发展离不开化学。
①陶瓷、水泥和普通玻璃都是生活中最常见的材料,它们属于 (填字母)。
a.金属材料
b.无机非金属材料
c.有机高分子材料[来源:学科网]
制造普通玻璃时,需要的主要原料有纯碱、石灰石和 (填化学式)。
②钢铁制品在潮湿的空气中发生 (填“化学”或“电化学”)腐蚀是造成钢铁腐蚀的主要原因。硬铝(一种铝合金)是制造飞机和宇宙飞船的理想材料,和纯铝相比,硬铝的强度 (填“低”、“高”或“无法确定”),具有较强的抗腐蚀能力。
③“白色污染”已成为当今社会的一大公害,“白色污染”主要是 (填“废塑料制品”、“废橡胶制品”或“生活垃圾”)造成的。在尼龙、棉花、涤纶这三种物质中,属于天然纤维的是 。橡胶是制造轮胎的重要原料,天然橡胶通过 (填“硫化”、“氧化”或“老化”)措施可增大其强度、弹性和化学稳定性等。
查看答案和解析>>
科目:高中化学 来源: 题型:
2014年1月4日,国家减灾办、民政部首次将危害健康的雾霾天气纳入2013年自然灾情进行通报。雾霾的形成与汽车尾气和燃煤有直接的关系,新近出版的《前沿科学》杂志刊发的中国环境科学研究院研究员的论文《汽车尾气污染及其危害》,其中系统地阐述了汽车尾气排放对大气环境及人体健康造成的严重危害。
(1)用SO2气体可以消除汽车尾气中NO2, 已知NO2(g)+SO2(g) SO3(g)+NO(g)
SO3(g)+NO(g)
一定条件下,将NO2与SO2以体积比1∶2置于体积为1L 密闭容器中发生上述反应,下列能说明反应达到平衡状态的是 。
a.体系压强保持不变 b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变 d.每消耗1 mol SO3的同时生成1 mol NO2
测得上述反应平衡时NO2与SO2体积比为1∶6,则平衡常数K= 。
(2)目前降低尾气中的NO和CO可行方法是在汽车排气管上安装催化转化器。NO和CO在催化转换器中发生反应:
2CO(g)+2NO(g) N2(g)+2CO2(g) △H=-a kJ·mol-1。
N2(g)+2CO2(g) △H=-a kJ·mol-1。
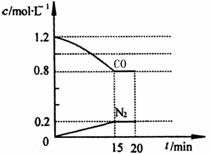 在25℃和101kPa下,将2.0mol NO、2.4mol气体
在25℃和101kPa下,将2.0mol NO、2.4mol气体
CO通入到固定容积为2L的容器中,反应过程中部分物
质的浓度变化如右图所示:
①有害气体NO的转化率为 ,0—15min
NO的平均速率v(NO)= mol/(L·min)。
②20min时,若改变反应条件,导致CO浓度减小,
则改变的条件可能是 (选填序号)。
 a.缩小容器体积 b.增加CO的量 c.降低温度 d.扩大容器体积
a.缩小容器体积 b.增加CO的量 c.降低温度 d.扩大容器体积
③如图所示,无摩擦、无质量的活塞1、2将反应器隔
成甲、乙两部分,在25℃和101kPa下实现平衡时,各部分
体积分别为V甲、V乙。此时若去掉活塞1,不引起活塞2的移
动。则x= ,V甲:V乙=
(3)消除汽车尾气中NO2也可以用CO,已知2NO(g)+O2(g)=2NO2(g) △H=-b kJ·mol-1;CO的燃烧热△H=-c kJ·mol-1。写处消除汽车尾气中NO2的污染时,NO2与CO的反应的热化学反应方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
科学家在2000年8月10日出版的英国《自然》杂志上报告,他们用DNA制造出了一种臂长只有7纳米的纳米级镊子,以便能够钳起分子或原子并对它们随意组合。下列分散系中的分散质的粒子直径与纳米级镊子臂长具有相同数量级的是( )
A. 溶液 B. 悬浊液 C. 乳浊液 D. 胶体
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:甲、乙、丙为常见单质,甲常温下为固体,乙为一黄绿色气体,丙为无色气体。A、B、C、D均为化合物,D为红褐色沉淀,它们之间有下图转化关系。请回答以下问题。
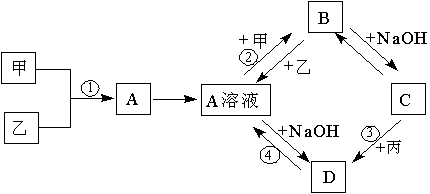
(1)写出下列物质的化学式;乙 ;B 。
(2)写出③反应的化学方程式 。
现象为 。
(3)写出②反应的离子方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
硝酸是一种具有强氧化性、强腐蚀性的无机酸,在储运过程中要严防泄漏。回答下列有关问题:
(1)硝酸是一种强酸,并且具有强的氧化性,一般在运输浓硝酸时采用的储藏罐材料是____________(填序号),原因是______________________________。
①铁 ②铜 ③铝 ④陶瓷
(2)对于硝酸的泄漏事故,必须采取正确的处理方法,由于硝酸泄漏出后与其他物质发生反应,放出大量的热,可能会导致车轮胎等着火,甚至可能会引发油罐爆炸,故要及时用水降温,另外可以在地面铺撒________(选填①氯化钙、②熟石灰、③生石灰、④石灰石粉末、⑤氯化钠),目的是_______________________________。
用铁粉可以吗?________________________________,原因是________________________________________________________________________。
(3)硝酸本来无色,但硝酸有挥发性,挥发出来的硝酸遇空气中的水蒸气形成白雾,白雾的成分是________。而实际情况并非如此,从硝酸泄漏现场可以看到大量的红棕色气体弥漫,该红棕色气体的成分是______________;用化学方程式表示产生这种现象的原因____________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com