
【题目】如图所示,A是由导热材料制成的密闭容器,B是一耐化学腐蚀且易于传热的透明气囊.关闭K2 , 将各1mol NO2通过K1、K3分别充入A、B中,反应起始时A、B的体积相同均为a L. 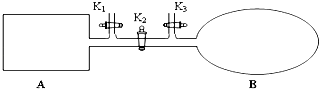
①B中可通过判断可逆反应2NO2N2O4已经达到平衡.
②若平衡后在A容器中再充入0.5mol N2O4 , 则重新到达平衡后,平衡混合气中NO2的体积分数(填“变大”“变小”或“不变”).
③若容器A中到达平衡所需时间t s,达到平衡后容器内压强为起始压强的0.8倍,则平均化学反应速率v(NO2)等于
④若打开K2 , 平衡后B容器的体积缩至0.4a L,则打开K2之前,气球B体积为L.
【答案】气囊不再变小或颜色不再变化;变小;![]() mol/(L?s);0.7a
mol/(L?s);0.7a
【解析】解:①B是一个气体压强不变的容器,所以当反应达到平衡状态时,混合气体的颜色和气囊体积不再改变,
所以答案是:气囊不再变小或颜色不再变化;
②再加入气体,相当于增大压强,化学平衡正向移动,二氧化氮的百分含量会减小,所以答案是:变小;
③2NO2N2O4
初始物质的量:1 0
变化的物质的量:2x x
平衡物质的量:1﹣2x x
则 ![]() =0.8,解得x=0.2mol,
=0.8,解得x=0.2mol,
所以平均化学反应速率v(NO2)= ![]() mol/(Ls)=
mol/(Ls)= ![]() mol/(Ls),
mol/(Ls),
所以答案是: ![]() mol/(Ls);
mol/(Ls);
④打开K2 , 则相当于是在等温等压时的平衡,因此平衡时等效的.由于此时反应物的物质的量是B中的二倍,所以打开K2之前,气球B体积为(aL+0.4aL)÷2=0.7aL,
所以答案是:0.7a.
【考点精析】解答此题的关键在于理解化学平衡状态本质及特征的相关知识,掌握化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效),以及对化学平衡的计算的理解,了解反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%.


科目:高中化学 来源: 题型:
【题目】工业合成氨反应的能量变化如图所示. 
(1)写出合成氨反应的热化学方程式:
(2)在甲乙两个体积均为2L固定容积的密闭容器中,分别充入甲:1molN2、3molH2和乙:1molN2、3molH2、1molHe,(其它条件相同),反应速率甲乙(填大于、小于或等于),经过足够长的时间后在甲容器中该反应放出的热量(或吸收的热量)92.4kJ(填“大于”、“小于”或“等于”)
(3)下列图象分别代表焓变(△H )、混合气体平均相对分子质量( ![]() )、N2体积分数
)、N2体积分数
φ(N2)和气体密度(ρ)与反应时间关系,其中正确且能表明该可逆反应达到平衡状态的是 . 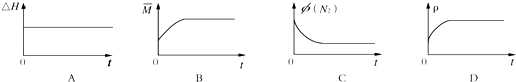
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2015年雾霾天气多次肆虐我国中东部地区.其中,汽车尾气和燃煤尾气是造成空气污染的原因之一.
(1)汽车尾气净化的主要原理为:2NO(g)+2CO (g) ![]() 2CO2 (g)+N2 (g)在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图1所示.
2CO2 (g)+N2 (g)在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图1所示. 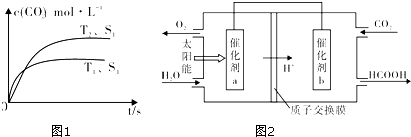
据此判断:
①该反应的平衡常数表达式为 .
②该反应的△H0(选填“>”、“<”).
③当固体催化剂的质量一定时,增大其表面积可提高化学反应速率.若催化剂的表面积S1>S2 , 在右图中画出c(CO2)在T2、S2条件下达到平衡过程中的变化曲线.
(2)直接排放煤燃烧产生的烟气会引起严重的环境问题.
①煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染.
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=﹣867kJmol﹣1
2NO2(g)N2O4(g)△H=﹣56.9kJmol﹣1
写出CH4催化还原N2O4(g)生成N2(g)、CO2(g)和H2O(g)的热化学方程式 .
②将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的.图2是通过光电转化原理以廉价原料制备新产品的示意图.写出上述光电转化过程的化学反应方程式 . 催化剂a、b之间连接导线上电子流动方向是(填a→b或b→a).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将0.1mo1L﹣1的醋酸溶液加水稀释至原来体积的10倍,下列有关叙述正确的是( )
A.CH3COOH的电离平衡常数增大为原来的10倍
B.CH3COO﹣与CH3COOH的浓度之比增大为原来的10倍
C.CH3COO﹣与H+的浓度之积减小为原来的0.1
D.CH3COOH与CH3COO﹣的浓度之和减小为原来的0.1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C三种物质各15g,它们发生反应时,只生成30g新物质D。若增加10gC时,A与C恰好完全反应,则A与B参加反应质量之比为
A.1:1 B.2:1 C.2:3 D.3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组用下列装置进行乙醇催化氧化的实验。
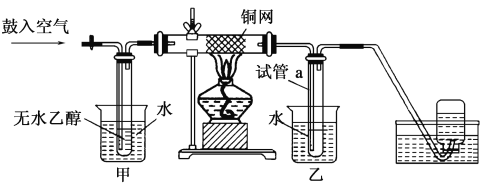
(1)实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学反应方程式:__________________。
在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇的氧化反应是________反应。
(2)甲和乙两个水浴作用不相同。
甲的作用是________;乙的作用是________。
(3)反应进行一段时间后,干燥试管a中能收集到不同的物质,它们是________。集气瓶中收集到的气体的主要成分是________。
(4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有________。要除去该物质,可先在混合液中加入________(填写字母)。
a.氯化钠溶液 b.苯
c.碳酸氢钠溶液 d.四氯化碳
然后,再通过________(填实验操作名称)即可除去。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,甲、乙是电化学实验装置,请回答下列问题: 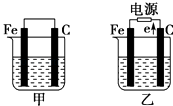
(1)若甲、乙两个烧杯中均盛放饱和NaCl溶液.
①甲中石墨棒上的电极反应式是 .
②将湿润的淀粉KI试纸放在乙烧杯的上方,发现试纸先变蓝后褪色,这是因为电解生成的某种气体A氧化了I﹣生成了I2 . 若A气体和I2按物质的量之比为5:1反应,且生成两种酸,该反应的化学方程式为 .
③如果不考虑气体产物与烧杯中溶液之间的反应,当乙反应有0.01mol电子转移后停止实验,烧杯中溶液的体积为100mL,则溶液混匀后的pH=
(2)若甲、乙两烧杯中均盛放CuSO4溶液.
①甲中铁棒上的电极反应式为 .
②乙中总反应的离子方程式为 .
③如果起始时乙中盛放100mL pH=5的CuSO4溶液(25℃),一段时间后溶液的pH变为1,若要使溶液恢复到起始时的浓度(忽略溶液体积的变化),可向溶液中加入(填写物质的化学式)g.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知硫﹣氨热化学循环分解水的示意图如图1: 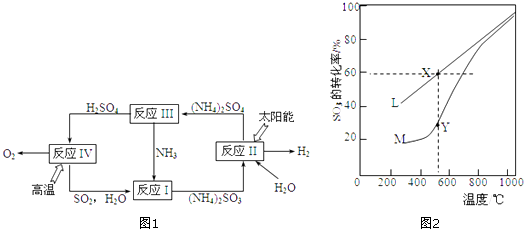
(1)从反应物和生成物的角度来看反应I属于(填序号). a.离子反应 b.化合反应 c.中和反应 d.氧化还原反应
(2)反应II是将太阳能转化为电能,再进行电解,电解池阳极的反应式是 .
(3)反应IV是由(a)、(b)两步反应组成: H2SO4(l)═SO3(g)+H2O(g)△H=+177kJmol﹣1 (a)
2SO3(g)2SO2(g)+O2(g)△H=+196kJmol﹣1 (b)
H2O(l)═H2O(g)△H=+44kJmol﹣1 (c)
H2SO4(l)分解为SO2(g)、O2(g)及H2O(l)的热化学方程式为: .
提高H2SO4(l)的分解率的方法是(写两种) .
(4)恒温恒容的密闭容器中进行不同温度下的SO3分解实验[原理按反应(b)].SO3起始物质的量均为dmol,图2中L曲线为SO3的平衡转化率与温度的关系,M曲线表示不同温度下反应经过相同反应时间且未达到化学平衡时SO3的转化率. ①Y点对应温度下的反应速率:v(正)v(逆)(选填:>,<,=);随温度的升高,M曲线逼近L曲线的原因是:
②若X点时总压为0.1MPa,列式计算SO3分解反应在图中X点的平衡常数Kp=(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,保留2位有效数字).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com