
在某温度时,测得纯水中的c(H+)=2.4×10-7 mol/L,则c(OH-)为( )
| A.2.4×10-7 mol/L | B.1.0×10-7 mol/L |
C.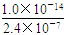 mol/L mol/L | D.c(OH-)无法确定 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| c(H+).c(Cl-).c(HClO) |
| C(Cl2) |
| 0.03×0.03×0.03 |
| 0.06 |
| c(H+).c(Cl-).c(HClO) |
| C(Cl2) |
| 0.03×0.03×0.03 |
| 0.06 |
查看答案和解析>>
科目:高中化学 来源: 题型:
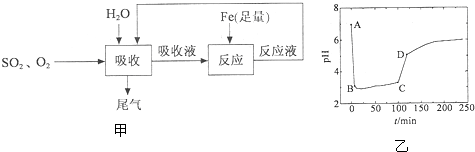
查看答案和解析>>
科目:高中化学 来源: 题型:
B.0.1×10-7mol·L-1?
C.![]() mol·L-1
mol·L-1
D.无法确定
查看答案和解析>>
科目:高中化学 来源:2011-2012学年浙江省湖州市高二(下)期末化学试卷(解析版) 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:
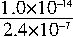 mol?L-1 D.无法确定
mol?L-1 D.无法确定查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com