
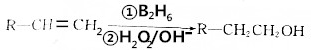
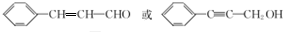 .
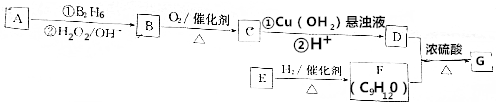
.分析 1molA充分燃烧可生成72g水,水的物质的量为$\frac{72g}{18g/mol}$=4mol,故A分子中H原子说明为8,烃A的相对分子质量为56,则A分子中C原子数目为$\frac{56-8}{12}$=4,故A的分子式为C4H8.A发生信息④中的反应得到B为醇,则B能连续氧化生成D,D的核磁共振氢谱有3组峰,则A为(CH3)2C=CH2,B为(CH3)2CHCH2OH,C为(CH3)2CHCHO,D为(CH3)2 CHCOOH.F的分子式为:C9H12O,分子中含有苯环且无甲基,则F为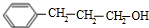 ,F与D发生酯化反应生成G为
,F与D发生酯化反应生成G为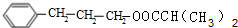 .在催化剂存在的条件下1mol E与2molH2可发生加成反应生成F,则E为
.在催化剂存在的条件下1mol E与2molH2可发生加成反应生成F,则E为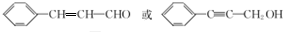 .
.
解答 解:1molA充分燃烧可生成72g水,水的物质的量为$\frac{72g}{18g/mol}$=4mol,故A分子中H原子说明为8,烃A的相对分子质量为56,则A分子中C原子数目为$\frac{56-8}{12}$=4,故A的分子式为C4H8.A发生信息④中的反应得到B为醇,则B能连续氧化生成D,D的核磁共振氢谱有3组峰,则A为(CH3)2C=CH2,B为(CH3)2CHCH2OH,C为(CH3)2CHCHO,D为(CH3)2 CHCOOH.F的分子式为:C9H12O,分子中含有苯环且无甲基,则F为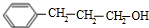 ,F与D发生酯化反应生成G为
,F与D发生酯化反应生成G为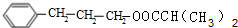 .在催化剂存在的条件下1mol E与2molH2可发生加成反应生成F,则E为
.在催化剂存在的条件下1mol E与2molH2可发生加成反应生成F,则E为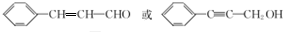 .
.
(1)A为(CH3)2C=CH2,名称为2-甲基-1-丙烯,
故答案为:2-甲基-1-丙烯;
(2)由B生成C的化学方程式为:2 (CH3)2CHCH2OH+O2$→_{△}^{Cu}$2 (CH3)2CHCHO+2H2O,
故答案为:2 (CH3)2CHCH2OH+O2$→_{△}^{Cu}$2 (CH3)2CHCHO+2H2O;
(3)G为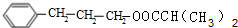 ,分子式为C13H18O2,D与F反应生成G的反应类型为酯化反应或取代反应,
,分子式为C13H18O2,D与F反应生成G的反应类型为酯化反应或取代反应,
故答案为:C13H18O2;酯化反应或取代反应;
(4)E的结构简式可能为: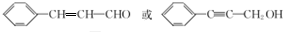 ,
,
故答案为: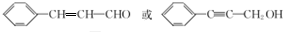 ;
;
(5)F(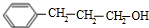 )有多种同分异构体,其中遇FeCl3溶液显紫色且苯环上只有两个取代基,其中一个取代基为-OH,另外取代基为-CH(CH3)2,或者-CH2CH2 CH3,各有邻、间、对3种,共有6种,
)有多种同分异构体,其中遇FeCl3溶液显紫色且苯环上只有两个取代基,其中一个取代基为-OH,另外取代基为-CH(CH3)2,或者-CH2CH2 CH3,各有邻、间、对3种,共有6种,
故答案为:6.
点评 本题考查有机物的推断,充分利用反应条件进行推断,熟练掌握官能团的性质与转化,注意对题目信息的理解,是对有机化学基础的综合考查.


 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案科目:高中化学 来源: 题型:选择题
 某同学按如图所示的装置进行实验.A、B为两种常见金属,它们的硫酸盐可溶于水.当K闭合时,在交換膜处
某同学按如图所示的装置进行实验.A、B为两种常见金属,它们的硫酸盐可溶于水.当K闭合时,在交換膜处| A. | 反应初期,x电极周围出现白色胶状沉淀,不久沉淀溶解 | |
| B. | 溶液中(A2+)减小 | |
| C. | y电极上有H2产生,发生还原反应 | |
| D. | B的电极反应:B-2e═B2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
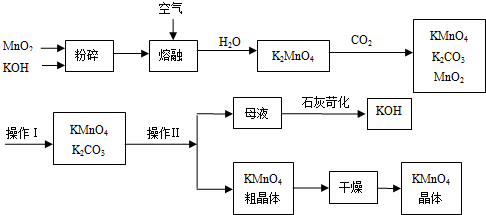
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2具有很强的氧化性,在化学反应中只能作氧化剂 | |
| B. | 液氨汽化时要吸收大量的热,可用作制冷剂 | |
| C. | 二氧化硅不与强酸反应,可用石英器皿盛放氢氟酸 | |
| D. | SO2和Cl2都有漂白作用,将等物质的量的两种气体同时作用于潮湿的有色物质时,可增强漂白作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子数和质量分别不等 | B. | 质子数相等,质量不等 | ||
| C. | 分子数和质量都相等 | D. | 原子数、中子数和质子数都相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl | |
| B. | CH2=CH2+HBr→CH3CH2Br | |
| C. | 2CH3CH2OH+2Na→2 CH3CH2ONa+H2↑ | |
| D. | 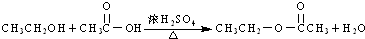 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | |
| B |
| A. | 铍能与冷水发生剧烈反应 | |
| B. | 氢氧化铍既能与强酸溶液反应,又能与强碱溶液反应 | |
| C. | 氢氧化铍的化学式为Be(OH)3 | |
| D. | 氧化铍只溶于强酸溶液,不溶于强碱溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com