
| A. | CO2、SiO2的晶体结构类型不同 | |
| B. | 加热硅、硫晶体使之熔化,克服的作用力不同 | |
| C. | HCl、NaCl溶于水,破坏的化学键类型相同 | |
| D. | NaOH、NH4Cl晶体中既有离子键又有共价键 |
分析 A.根据晶体的构成微粒判断;
B.加热熔化时原子晶体克服共价键,分子晶体克服分子间作用力;
C.离子化合物中含有离子键,共价化合物中只含有共价键;
D.阴阳离子间形成离子键,非金属原子间形成共价键.
解答 解:A.CO2晶体中分子间通过分子间作用力结合为分子晶体,SiO2晶体中Si与O原子间通过共价键结合形成原子晶体,晶体结构类型不同,故A正确;
B.硅属于原子晶体,加热熔化时原子晶体克服共价键,S属于分子晶体,分子晶体克服分子间作用力,则加热硅、硫晶体使之熔化,克服的作用力不同,故B正确;
C.HCl属于共价化合物溶于水电离,破坏共价键,NaCl属于离子化合物,溶于水破坏离子键,故C错误;
D.NaOH中钠离子与氢氧根离子形成离子键,O与H形成共价键,NH4Cl晶体中铵根离子与氯离子形成离子键,N与H形成共价键,既有离子键又有共价键,故D正确.
故选C.
点评 本题考查了共价键和离子键、晶体类型的判断、分子间作用力等,题目难度不大,注意把握共价键和离子键的概念以及化学键与分子间作用力的区别.


 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案科目:高中化学 来源: 题型:实验题
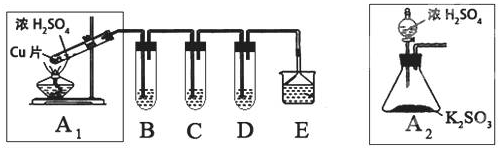
| 实验操作 | 预期现象与结论 |
| 步骤1:取适量“吸收液”于小烧杯中,用胶头滴管取1mol/L BaCl2溶液向小烧杯滴加直至过量. | 若出现白色浑浊,则溶液中存在SO32-或 SO42-. |
| 步骤2:将小烧杯中的浊液过滤、洗涤,再用适量水把附在滤纸上的固体冲入另一小烧杯中;向冲下的固体滴入1滴(或少量)品红,再滴入过量2mol/L盐酸,振荡. | |
| 步骤3:用试管取适量滤液,向其中(或小烧杯中)滴入过量的1mol/LBa(OH)2溶液[或滴入1滴(或少量)品红溶液,再滴入2-3滴(或过量)的2mol/L盐酸],振荡 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤的干馏是化学变化,而煤的气化、液化是物理变化 | |
| B. | 石油裂解是为了获得更多汽油,以满足迅速增长的汽车需要 | |
| C. | 氢能、电能、风能都是无毒、无污染的绿色新能源,可以安全使用 | |
| D. | 玻璃是将石灰石、纯碱、石英在玻璃熔炉中高温熔融制得的 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
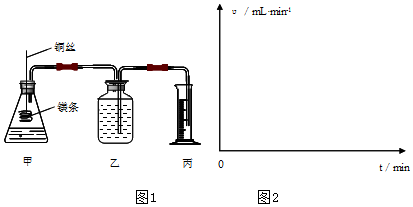
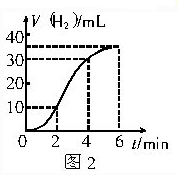
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含大量OH-的溶液:Ba2+、K+、NO3-、AlO2- | |
| B. | 加人Na2O2粉末的溶液:Na+、Cl-、SO32-、OH- | |
| C. | c(KNO3)=1.0mol/L的溶液:H+、I-、Cl-、Ca2+ | |
| D. | 滴入紫色石蕊试液呈蓝色的溶液:Fe3+、Ba2+、HCO3-、Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
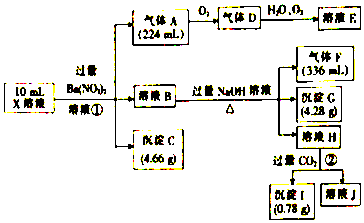
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢元素是还原剂 | B. | O2是氧化剂 | C. | H2发生氧化反应 | D. | O2被还原 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 六氟化氙(XeF6) | B. | 次氯酸(HClO) | C. | 氯化硫(S2Cl2) | D. | 白磷(P4) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com