
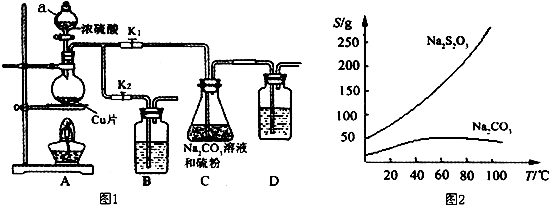
分析 (1)步骤1:利用气体热胀冷缩性质,检验装置气密性;
步骤2:装置B、D的作用是进行尾气处理,防止尾气中二氧化硫污染空气;
步骤3:硫代硫酸钠在酸性溶液中不稳定,应控制溶液为弱碱性,即控制溶液pH接近或不小于7;
步骤4:从溶液中获得晶体,需要加热浓缩,趁热过滤,再将滤液冷却结晶、过滤、洗涤、烘干,得到产品;
(2)由题目信息可知,Na2S2O3被氯水氧化反应生成Na2SO4、H2SO4,氯气被还原为HCl;
(3)由题意可知,BaCrO4用盐酸溶解转化为Cr2O2-7,由元素守恒及已知方程式可得关系式:2Ba2+~2BaCrO4~Cr2O2-7~3I2~6Na2S2O3,结合消耗的Na2S2O3利用关系式计算溶液中n(Ba2+),进而计算c(Ba2+).
解答 解:(1)步骤1:利用气体热胀冷缩性质,检验装置气密性,具体操作为:关闭K2打开K1,在D中加水淹没导管末端,用热毛巾或双手捂住烧瓶,D中导管有气泡冒出,冷却后形成1段水柱,说明气密性良好;故答案为:关闭K2打开K1,在D中加水淹没导管末端,用热毛巾或双手捂住烧瓶,D中导管有气泡冒出,冷却后形成1段水柱,说明气密性良好;
步骤2:装置B、D的作用是进行尾气处理,防止尾气中二氧化硫污染空气,二氧化硫具有还原性,可以用酸性高锰酸钾溶液氧化吸收,二氧化硫能与氢氧化钠溶液、碳酸氢钠溶液反应被吸收,故选:ACD;
步骤3:硫代硫酸钠在酸性溶液中不稳定,应控制溶液为弱碱性,可以控制溶液pH接近或不小于7,
步骤4:从溶液中获得晶体,需要加热浓缩,趁热过滤,再将滤液冷却结晶、过滤、洗涤、烘干,得到产品,
故答案为:冷却结晶;
(2)由题目信息可知,Na2S2O3被氯水氧化反应生成Na2SO4、H2SO4,氯气被还原为HCl,反应方程式为:Na2 S2O3+4Cl2+5H2O=Na2SO4+H2SO4+8HCl,
故答案为:Na2 S2O3+4Cl2+5H2O=Na2SO4+H2SO4+8HCl;
(3)由题意可知,BaCrO4用盐酸溶解转化为Cr2O2-7,由元素守恒及已知方程式可得关系式:2Ba2+~2BaCrO4~Cr2O2-7~3I2~6Na2S2O3,消耗的Na2S2O3为0.018L×0.01mol/L,则n(Ba2+)=0.018L×0.01mol/L×$\frac{1}{3}$=0.00006mol,故溶液中c(Ba2+)=$\frac{0.00006mol}{0.025L}$=0.0024mol/L,
故答案为:0.0024mol/L.
点评 本题考查实验制备方案设计,涉及气密性检验、对实验装置及步骤的分析评价、物质的分离提纯、氧化还原反应滴定,(3)中注意利用关系式进行计算,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 制取乙烯:乙醇与浓硫酸共热至140℃ | |
| B. | 除去甲烷中的乙炔:混合气体通过酸性高锰酸钾溶液,再经浓硫酸干燥 | |
| C. | 除去苯中的苯酚:加入NaOH溶液振荡,静置分层后,除去水层 | |
| D. | 检验氯乙烷中的氯元素:氯乙烷与NaOH的水溶液共热后,加入AgNO3溶液有白色沉淀生成证明含CI- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 时间(min) 物质的量(mol) | 0 | 1 | 2 | 3 | 4 |
| X2 | 3.0 | n1 | 2.4 | n3 | n5 |
| H2 | 9.0 | 8.4 | 7.2 | n4 | n6 |
| XH3 | 0 | 0.4 | n2 | 2.0 | 2.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 萘(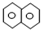 )是最简单的稠环芳香烃,萘与足量氢气充分加成的产物一氯代物有2种 )是最简单的稠环芳香烃,萘与足量氢气充分加成的产物一氯代物有2种 | |
| B. | 酚酞的结构如图所示,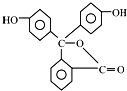 其结构中含有羟基(-OH),故酚酞属于醇 其结构中含有羟基(-OH),故酚酞属于醇 | |
| C. | 溴水能将甲苯、己烯、CCl4、乙醇四种溶液鉴别开来 | |
| D. | 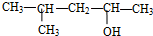 的名称为2-甲基-4-戊醇 的名称为2-甲基-4-戊醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下(如图)化合物.
乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下(如图)化合物. .
. 、
、 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实 验 内 容 | 实 验 试 剂 | 实 验 现 象 |
| 探究氧化性 | 取适量碘化钾淀粉溶液于试管中,加入过氧化氢溶液 | 溶液变蓝色 |
| 探究不稳定性 | 取适量过氧化氢溶液于试管中,加热, 用带火星的木条检验 | 产生气泡,木条复燃 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
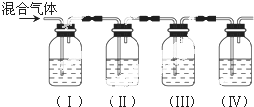
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 液态HF与液态HBr分别受热变为气体 | |
| B. | 氯化铵与苯分别受热变为气体 | |
| C. | 氯化钠与氯化氢分别溶解在水中 | |
| D. | 碘与干冰分别受热变为气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
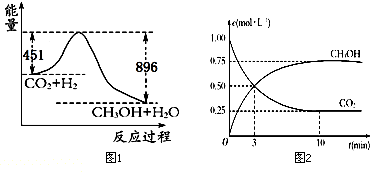
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com