
| CuO、CuCl2 |
| 400℃ |



 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案科目:高中化学 来源: 题型:
 如图,将2mL浓度为6mol/L的盐酸用注射器通过橡皮塞慢慢注入,玻璃管中出现小气泡,气泡在溶液中逐渐上升的过程中消失.对该反应过程的推断不合理的是( )
如图,将2mL浓度为6mol/L的盐酸用注射器通过橡皮塞慢慢注入,玻璃管中出现小气泡,气泡在溶液中逐渐上升的过程中消失.对该反应过程的推断不合理的是( )| A、有反应CO32-+2H+=CO2↑+H2O发生 |
| B、有反应CO32-+H+=HCO3-发生 |
| C、有反应CO32-+CO2+H2O=2HCO3-发生 |
| D、加快盐酸注入速度不会改变反应现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 高温、高压 |
| 催化剂 |
容器 |
甲 | 乙 | 丙 |
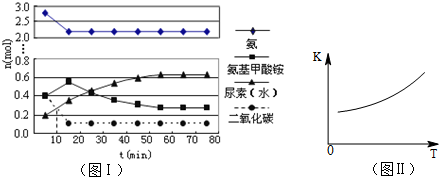
| 反应物投入量 | 3mol H2、2mol N2 | 6mol H2、4mol N2 | 2mol NH3 |
| 达到平衡的时间/min | 5 | 8 | |
| 平衡时N2的浓度/mol?L-1 | c1 | 1.5 | |
| NH3的体积分数 | ω1 | ω3 | |
| 混合气体密度/g?L-1 | ρ1 | ρ2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铝与盐酸反应:Al+H+=Al3++H2↑ |
| B、氢氧化铝与氢氧化钠溶液反应:Al(OH)3+OH-=AlO2-+2H2O |
| C、铁与氯化铁溶液反应:Fe+Fe3+=2Fe2+ |
| D、铝与氢氧化钠溶液反应:Al+2 OH-=AlO2-+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 工业上利用CO和水蒸气在一定条件下发生反应制取氢气.
工业上利用CO和水蒸气在一定条件下发生反应制取氢气.| 温度/℃ | 500 | 600 | 850 |
| 平衡常数K | 10 | 9 | 1 |
| 容器编号 | 起始时各物质物质的量(单位:mol) | 达到平衡时H2的体积分数 | 结论 | |||
| CO | H2O | CO2 | H2 | |||
| 1 | 1 | 4 | 0 | 0 | ||
| 2 | 2 | 8 | 0 | 0 | ||
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| O | - 4 |
| O | - 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在25°C、1.01×105Pa时,11.2氮气所含的原子数目为NA |
| B、18g水所含的电子数目为NA |
| C、121gCCl2F2所含的氯原子数为2NA |
| D、醋酸的摩尔质量与NA个醋酸分子的质量在数值上不相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com