
【题目】如图所示为与水相关的部分转化关系(水作反应物或生成物,部分产物和反应条件未列出).下列说法错误的是( ) 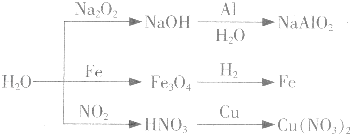
A.如图所示的反应均为氧化还原反应
B.比较镁、铁与水的反应条件,可知铁的金属性比镁弱
C.工业上常用NO2与水的反应原理制取硝酸
D.实验室中可用铜与稀硝酸反应制取NO2
科目:高中化学 来源: 题型:
【题目】将1mol纯净的A置于真空密闭容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其分解达到平衡:A(s)![]() 2B(g) +C(g),下列可以判断该反应已达到化学平衡状态的是
2B(g) +C(g),下列可以判断该反应已达到化学平衡状态的是
A. 反应速率:vB(正)=vc(逆) B. B的体积分数不变
C. 气体的密度保持不变 D. 混合气体的平均摩尔质量保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期元素在周期表中的位置如图,其中只有M元素原子最外层电子数与电子层数相等,下列说法不正确的是( ) 
A.原子半径Z<M
B.Y的最高价氧化物对应水化物的酸性比X的弱
C.非金属性:X<Z
D.M元素最高价氧化物对应水化物具有两性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知β锂辉矿(主要成分为LiAlSi2O6 , 还含有FeO、MgO、CaO等杂质),下面是以锂辉矿为原料来制取金属锂的一种工艺流程.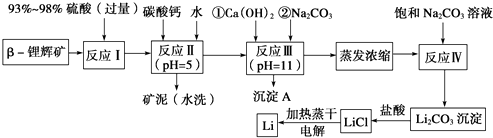
已知:①部分金属氢氧化物开始沉淀和完全沉淀时的pH:
氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
开始沉淀pH | 2.7 | 3.7 | 9.6 |
完全沉淀pH | 3.7 | 4.7 | 11 |
②Li2CO3在不同温度下的溶解度如下表:
温度/℃ | 0 | 10 | 20 | 50 | 75 | 100 |
Li2CO3的溶解度/g | 1.539 | 1.406 | 1.329 | 1.181 | 0.866 | 0.728 |
请回答下列问题:
(1)为了提高β锂辉矿浸出率可采取措施有 .
(2)反应Ⅰ发生主反应:LiAlSi2O6+H2SO4(浓Li2SO4+++H2O,根据题意配平上述方程式.
(3)反应Ⅱ加入碳酸钙的作用是 .
(4)反应Ⅲ中生成沉淀A成分: . (填化学式)
(5)蒸发浓缩过程中主要发生离子反应方程式: .
(6)洗涤所得Li2CO3沉淀要使用(选填“热水”或“冷水”),你选择的理由是 .
(7)电解熔融氯化锂生产锂时,阳极产生的Cl2中会混有少量O2 , 用电极反应式说明原因 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究性学习小组的同学们用如图所示装置进行铝热反应的实验,请回答: 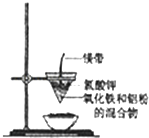
(1)氧化铁与铝反应的化学方程式是 ,
(2)镁带的作用是;氯酸钾的作用是 .
(3)同学们在实验过程中观察到纸漏斗的下部被烧穿,有熔融物落入沙中.他们为探究此熔融物的成分,查阅(化学手册)得知有关物质的熔点、沸点数据如下:
物质 | Al | Al2O3 | Fe | Fe2O3 |
熔点/℃ | 660 | 2054 | 1535 | 1462 |
沸点/℃ | 2467 | 2980 | 2750 | ﹣ |
同学们分析数据后推测该熔融物是一种合金,其中的金属是 , 溶解该合金可选用下列试剂中的(填序号).
A.FeSO4溶液 B.稀硫酸 C.稀硝酸 D.NaOH溶液.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的锌与100mL 18.5mol/L H2SO4充分反应后,锌完全溶解,同时生成气体A 22.4L(标准状况).将反应后的溶液稀释至1L,测得溶液的pH=1,则下列叙述中错误的是( )
A.气体A为SO2和H2的混合物
B.反应中共消耗Zn 65g
C.气体A中SO2和H2的体积比为1:4
D.反应中共转移电子2mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是元素周期表中短周期的一部分,若A原子最外层的电子数比次外层少3,则下列说法正确的是( )
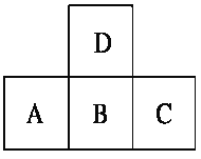
A. 原子半径的大小顺序是C > B > A > D
B. B、D之间只能形成一种化合物
C. 只有A的单质存在同素异形体
D. A、B、C的最高价氧化物对应水化物的酸性强弱的关系是C > B > A
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】市场上有一种加酶洗衣粉,即在洗衣粉中加入少量的碱性蛋白酶,它的催化活性很强,衣物的汗渍、血迹以及人体排放的蛋白质油渍等遇到它,皆能水解而除去.下列衣料中不能用加酶洗衣粉洗涤的是( )
①棉织品②毛织品③腈纶织品④蚕丝织品⑤涤纶织品⑥尼龙织品.
A.①②③
B.②④
C.③④⑤
D.③⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com