
烷烃C5H12的同分异构体数目是
A.2B.3C.4D.5
科目:高中化学 来源:2013-2014天津市高三毕业班联考二理综化学试卷(解析版) 题型:选择题
NA为阿伏加德罗常数的值。下列叙述正确的是
A.1.0 L 1.0 mol·L-1的NaClO水溶液中含有的氧原子数为NA
B.25 ℃时1L pH=13的Ba(OH)2溶液中含有OH-的数目为0.1NA
C.2.24 L 的2H35Cl分子中的中子数是1.9NA
D.某密闭容器中盛有0.1 mol N2和0.3 mol H2,在一定条件下充分反应,形成N—H键的数目为0.6NA
查看答案和解析>>
科目:高中化学 来源:2013-2014天津五区县高二下学期期末考试化学试卷(解析版) 题型:选择题
下列关于有机化合物的认识不正确的是
A.盐析可提纯蛋白质并保持其生理活性
B.蔗糖、麦芽糖的分子式都是C12H22O11,二者互为同分异构体
C.石油分馏可获得乙烯、丙烯和丁二烯
D.向澄清的苯酚钠溶液中通入二氧化碳气体,会看到澄清溶液变浑浊
查看答案和解析>>
科目:高中化学 来源:2013-2014天津五区县高一下学期期末考试化学试卷(解析版) 题型:选择题
某同学做完铜、锌稀硫酸原电池的实验后得出了下列结论,你认为正确的是
A.构成原电池正极和负极的材料必须是两种金属
B.当由铜、锌电极与硫酸铜溶液组成原电池时,铜是负极
C.该实验电子沿导线由锌流向铜,氢离子得到电子而放出氢气
D.铜锌原电池工作时,电流由锌经导线流向铜
查看答案和解析>>
科目:高中化学 来源:2013-2014天津五区县高一下学期期末考试化学试卷(解析版) 题型:选择题
下列各组液体混合物,能用分液漏斗分离的是
A.乙酸和水B.液溴和苯
C.苯和水D.乙醇和水
查看答案和解析>>
科目:高中化学 来源:2013-2014四川绵阳中学实验学校高考冲刺理综化学试卷(解析版) 题型:实验题
(15分)雾霾含有大量的污染物SO2、NO。工业上变“废”为宝,吸收工业尾气SO2和NO,可获得Na2S2O3和NH4NO3产品的流程图如下(Ce为铈元素):
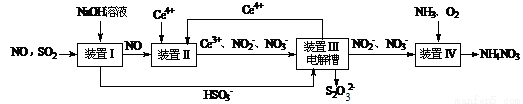
⑴装置Ⅰ中的主要离子方程式为 。3
⑵含硫各微粒(H2SO3、HSO3-和SO32-)存在于SO2与NaOH溶液反应后的溶液中,它们的物质的量分数X(i)与溶液pH 的关系如图所示。
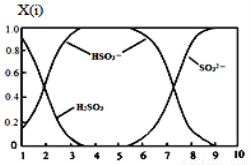

①若是0.1molNaOH反应后的溶液,测得溶液的pH=8时,溶液中个离子由大到小的顺序是 。
②向pH=5的NaHSO3溶液中滴加一定浓度的CaCl2溶液,溶液中出现浑浊,pH降为2,用化学平衡移动原理解释溶液pH降低的原因: 。
⑶写出装置Ⅱ中,酸性条件下的离子方程式 。
⑷装置Ⅲ还可以使Ce4+再生,其原理如下图所示。
①生成Ce4+从电解槽的 (填字母序号)口流出。②写出与阴极的反应式 。
⑸已知进入装置Ⅳ的溶液中,NO2-的浓度为a g·L-1,要使1 m3该溶液中的NO2-完全转化为NH4NO3,需至少向装置Ⅳ中通入标准状况下的O2 L。(用含a代数式表示, 计算结果保留整数)
查看答案和解析>>
科目:高中化学 来源:2013-2014四川绵阳中学实验学校高考冲刺理综化学试卷(解析版) 题型:选择题
下列实验能达到预期目的的是 ( )
编号 | 实验内容 | 实验目的 |
A | 室温下,用pH试纸分别测定浓度为0.1mol·L-1NaClO溶液和0.1mol·L-1CH3COONa溶液的pH | 比较HClO和CH3COOH的酸性强弱 |
B | 向含有酚酞的Na2CO3溶液中加入少量BaC12固体,溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
C | 向10mL 0.2 mol/L NaOH溶液中滴入2滴0.1 mol/L MgCl2溶液,产生白色沉淀后,再滴加2滴0.1 mol/LFeCl3溶液,又生成红褐色沉淀 | 证明在相同温度下的Ksp: Mg(OH)2 >Fe(OH)3 |
D | 分别测定室温下等物质的量浓度的Na2SO3与Na2CO3溶液的pH,后者较大 | 证明非金属性S>C |
查看答案和解析>>
科目:高中化学 来源:2013-2014四川省下学期期中考试高二化学试卷(解析版) 题型:填空题
(11分)甲、乙两池电极材料都是铁棒与碳棒,请回答下列问题:
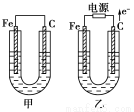
(1)若两池中均为CuSO4溶液,反应一段时间后:
①有红色物质析出的是甲池中的________棒,乙池中的________棒。
②乙池中阳极的电极反应式是_______________________________________________ _。
(2)若两池中均为饱和NaCl溶液:
①写出乙池中总反应的离子方程式__________________________________________。
②甲池中碳极上电极反应式是____________________,乙池中碳极上电极反应属于____________(填“氧化反应”或“还原反应”)。
③若乙池转移0.02 mol e-后停止实验,该池中溶液体积是200 mL,则溶液混匀后的pH=________。
查看答案和解析>>
科目:高中化学 来源:2013-2014四川省下学期期中考试高一化学试卷(解析版) 题型:选择题
下列说法中正确的是 ( )
A.6.8 g固体KHSO4与3.9 g固体Na2O2中阴离子数目相同
B.常温下铁、铜均不溶于浓硫酸, 说明常温下铁、铜与浓硫酸均不反应
C.离子化合物中只含离子键
D.中子数为18的氯原子可表示为18Cl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com