
分析 (1)二氧化硫具有还原性,能够与溴水发生氧化还原反应生成氢溴酸和硫酸而是溴水褪色;
(2)三价铁离子能够氧化碘离子生成单质碘和二价铁离子;
(3)0.75molCO2与1molNaOH溶液反应生成0.25molNa2CO3、0.5molNaHCO3;
(4)NaClO3与Na2SO3在H2SO4存在下生成二氧化氯和硫酸氢钠;
(5)H2O2和酸性KMnO4发生氧化还原反应生成锰离子、氧气;
(6)碳酸氢钠过量,氢氧化钙不足,反应按照氢氧化钙的量进行;
解答 解:(1)SO2使溴水褪色,二者发生氧化还原反应生成氢溴酸和硫酸,离子方程式:SO2+Br2+2H2O═4H++2Br-+SO42-;
故答案为:SO2+Br2+2H2O═4H++2Br-+SO42-;
(2)FeCl3溶液使淀粉KI溶液变蓝,是因为三价铁离子能够氧化碘离子生成单质碘和二价铁离子,离子方程式:2Fe3++2I-=I2+2Fe2+;
故答案为:2Fe3++2I-=I2+2Fe2+;
(3)0.75molCO2与1molNaOH溶液反应生成0.25molNa2CO3、0.5molNaHCO3,离子方程式:3CO2+4OH-=CO32-+2HCO3-+H2O;
故答案为:3CO2+4OH-=CO32-+2HCO3-+H2O,
(4)NaClO3与Na2SO3在H2SO4存在下生成二氧化氯和硫酸氢钠,离子方程式:2ClO3-+SO32-+2H+=2ClO2+SO42-+H2O;
故答案为:2ClO3-+SO32-+2H+=2ClO2+SO42-+H2O;
(5)H2O2和酸性KMnO4发生氧化还原反应生成锰离子、氧气,离子反应为2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O;
故答案为:2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O;
(6)澄清石灰水与过量小苏打溶液混合,碳酸氢钠过量,反应的离子方程式为:Ca2++2OH-+2HCO3-=CaCO3↓+CO32-+2H2O;
故答案为:Ca2++2OH-+2HCO3-=CaCO3↓+CO32-+2H2O;
点评 本题考查了离子方程式的书写,该题是高考中的高频题,属于中等难度的试题,侧重对学生能力的培养和训练,明确物质的性质及发生反应的实质是解题关键,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 成份 | 浓度/(mol•L-1) | 质量分数 |
| HCl FeCl2 FeCl3 | -- 1.920 0.071 | 5.00% 8.94% 0.33% |
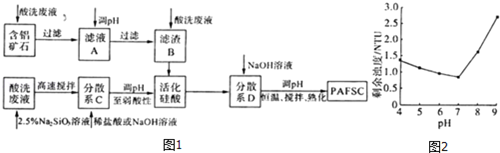
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,23gNO2与N2O4的混合物中含有NA个氧原子 | |
| B. | 一定条件下,1.4g N2和0.2mol H2混合充分反应,转移的电子数为0.3NA | |
| C. | 标准状况下,40g三氧化硫体积约为11.2L | |
| D. | 1L1mol•L?1的Na2CO3 溶液中阴离子数目小于NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1H、D+、T2互为同位素 | |
| B. | 金属单质都能导电,非金属单质都不能导电 | |
| C. | 非金属元素最高价氧化物的水化物并不一定都具有强氧化性 | |
| D. | 非金属氧化物不一定是酸性氧化物,而金属氧化物一定是碱性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K2CO3→KOH | B. | Fe2O3→Fe (OH)3 | C. | Zn→ZnCl2 | D. | MgCl2→Mg(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L 氟化氢中含2NA个原子 | |
| B. | 0.1mol/L的Na2CO3溶液含有CO32-的数目为0.1NA | |
| C. | 6.0g金刚石含有C-C键的数目为NA | |
| D. | 氢氧燃料电池正极消耗22.4 L气体时,电路中通过电子的数目为4 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④ | B. | ①④ | C. | ②③ | D. | ③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com