
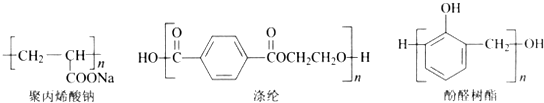
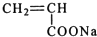 ,反应类型是加聚反应;
,反应类型是加聚反应;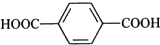 ,其核磁共振氢谱的峰面积比是1:2(或2:1);
,其核磁共振氢谱的峰面积比是1:2(或2:1);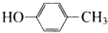 和乙醛在酸性条件下也可以发生类似于制备酚醛树脂的反应,此反应的化学方程式是
和乙醛在酸性条件下也可以发生类似于制备酚醛树脂的反应,此反应的化学方程式是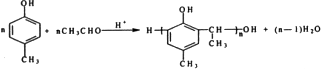 .
. 分析 (1)凡链节的主链上只有两个碳原子(无其它原子)的高聚物,其合成单体必为一种,将两半链闭合即可;
(2)涤纶 是由对苯二甲酸和乙二醇缩聚而成;羧基能和NaHCO3反应;核磁共振氢谱的峰面积比等于氢原子数之比;
是由对苯二甲酸和乙二醇缩聚而成;羧基能和NaHCO3反应;核磁共振氢谱的峰面积比等于氢原子数之比;
(3)①合成酚醛树脂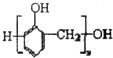 的单体是苯酚和甲醛;
的单体是苯酚和甲醛;
②苯酚与甲醛在酸性条件下聚合生成线型酚醛树脂;
③酚醛树脂是由苯酚和甲醛在催化剂条件下缩聚而成,反应机理是苯酚羟基邻位上的两个氢原子比较活泼,与甲醛醛基上的氧原子结合为水分子,其余部分连接起来成为高分子化合物.
解答 解:(1)合成聚丙烯酸钠的单体的结构简式是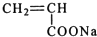 ,该反应是加聚反应,故答案为:
,该反应是加聚反应,故答案为: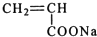 ;加聚反应;
;加聚反应;
(2)涤纶 是由对苯二甲酸和乙二醇缩聚而成;
是由对苯二甲酸和乙二醇缩聚而成; 能和NaHCO3反应,核磁共振氢谱的峰面积比是1:2,故答案为:
能和NaHCO3反应,核磁共振氢谱的峰面积比是1:2,故答案为: ;1:2(或2:1);
;1:2(或2:1);
(3)①合成酚醛树脂 的单体是苯酚和甲醛.苯酚和甲醛能与氢气发生加成反应,钠能与苯酚反应,故答案为:a;
的单体是苯酚和甲醛.苯酚和甲醛能与氢气发生加成反应,钠能与苯酚反应,故答案为:a;
②苯酚与甲醛在酸性条件下聚合生成线型酚醛树脂,碱性条件下聚合生成体型酚醛树脂,线型酚醛树脂可以溶于乙醇,故答案为:a、c;
③ 和乙醛反应的方程式可以表示为:
和乙醛反应的方程式可以表示为: ,故答案为:
,故答案为: .
.
点评 本题考查聚合物寻找单体的方法以及有机物的性质,注意聚合反应的类型和方程式的书写,难度不大.


 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加成反应 | B. | 消去反应、氧化反应 | ||
| C. | 氧化反应、加成反应 | D. | 加成反应、取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
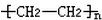 .
.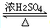 CH3COOC2H5+H2O,反应类型是酯化或取代反应.
CH3COOC2H5+H2O,反应类型是酯化或取代反应.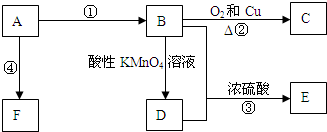
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
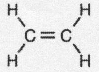 .
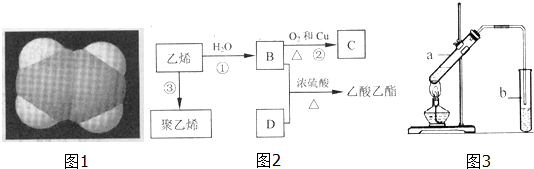
.
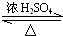 CH3COOC2H5+H2O.
CH3COOC2H5+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na | B. | Mg | C. | Al | D. | Zn |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com