
| ĪļÖŹ | CH3OH | CH3OCH3 | H2O |
| ÅضČ/£Ømol•L-1£© | 0.44 | 0.6 | 0.6 |
| A£® | a=1.64 | |
| B£® | “ĖŹ±Õż·“Ó¦ĖŁĀŹ“óÓŚÄę·“Ó¦ĖŁĀŹ | |
| C£® | ČōĘšŹ¼Ź±¼ÓČė2a mol CH3OH£¬Ōņ“ļµ½Ę½ŗāŹ±CH3OHµÄ×Ŗ»ÆĀŹŌö“ó | |
| D£® | Čō»ģŗĻĘųĢåµÄĘ½¾łÄ¦¶ūÖŹĮæ²»ŌŁ±ä»Æ£¬ŌņĖµĆ÷·“Ó¦ŅŃ“ļµ½Ę½ŗāדĢ¬ |
·ÖĪö ÓɱķÖŠŹż¾ŻæÉÖŖ£¬
2CH3OH£Øg£©?CH3OCH3£Øg£©+H2O£Øg£©
æŖŹ¼ $\frac{a}{2}$ 0 0
×Ŗ»Æ 1.2 0.6 0.6
ijŹ±æĢ 0.44 0.6 0.6
A.0.44+1.2=$\frac{a}{2}$£»
B£®Qc=$\frac{0.6”Į0.6}{0.4{4}^{2}}$=1.86£¼K£»
C£®ĪĀ¶Č²»±ä”¢Ģå»ż²»±ä£¬ĘšŹ¼ĮæĪŖŌĄ“µÄ2±¶£¬ĪŖµČŠ§Ę½ŗā£»
D£®ÓÉM=$\frac{m}{n}$æÉÖŖ£¬øĆ·“Ó¦ĪŖĘųĢåĢå»ż”¢ÖŹĮæ²»±äµÄ·“Ó¦£®
½ā“š ½ā£ŗÓɱķÖŠŹż¾ŻæÉÖŖ£¬
2CH3OH£Øg£©?CH3OCH3£Øg£©+H2O£Øg£©
æŖŹ¼ $\frac{a}{2}$ 0 0
×Ŗ»Æ 1.2 0.6 0.6
ijŹ±æĢ 0.44 0.6 0.6
A.0.44+1.2=$\frac{a}{2}$£¬½āµĆa=1.64”Į2=3.28mol£¬¹ŹA“ķĪó£»
B£®Qc=$\frac{0.6”Į0.6}{0.4{4}^{2}}$=1.86£¼K=400£¬æÉÖŖ·“ĻņÕż·“Ó¦·½Ļņ½ųŠŠ£¬¼“Õż·“Ó¦ĖŁĀŹ“óÓŚÄę·“Ó¦ĖŁĀŹ£¬¹ŹBÕżČ·£»
C£®øĆ·“Ó¦ĪŖĘųĢåĢå»ż²»±äµÄ·“Ó¦£¬ĘšŹ¼Ź±¼ÓČė2a mol CH3OHÓėĘšŹ¼Ź±¼ÓČėa mol CH3OH£¬ĖłµĆµ½µÄĘ½ŗāĪŖµČŠ§Ę½ŗā£¬CH3OHµÄ×Ŗ»ÆĀŹĻąµČ£¬¹ŹC“ķĪó£»
D£®øĆ·“Ó¦µÄĘųĢå×ÜÖŹĮæ²»±ä£¬×ÜĪļÖŹµÄĮæŅ²²»±ä£¬ĖłŅŌŌŚ·“Ó¦¹ż³ĢÖŠŗĻĘųĢåµÄĘ½¾łÄ¦¶ūÖŹĮæŹ¼ÖÕ²»±ä£¬ĖłŅŌ»ģŗĻĘųĢåµÄĘ½¾łÄ¦¶ūÖŹĮæ²»ŌŁ±ä»Æ£¬²»ÄÜĖµĆ÷·“Ó¦ŅŃ“ļµ½Ę½ŗāדĢ¬£¬¹ŹD“ķĪó£»
¹ŹŃ”B£®
µćĘĄ ±¾Ģāæ¼²é»ÆŃ§Ę½ŗāµÄ¼ĘĖć£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕ±ķøńŹż¾ŻµÄÓ¦ÓĆ”¢Ę½ŗāČż¶Ī·Ø”¢µČŠ§Ę½ŗāĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓė¼ĘĖćÄÜĮ¦µÄ漲飬עŅāQcµÄÓ¦ÓĆ£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | š¤½ŗĻĖĪ¬ | B£® | Āȶ”Ļš½ŗ | C£® | ¶ÆĪļ½ŗ | D£® | Ć«·¢ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Fe2O3-ŗŚÉ« | B£® | Na2O2-°×É« | C£® | CuSO4-°×É« | D£® | Fe£ØOH£©2-»ŅĀĢÉ« |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŃŖŗģµ°°×”¢Å£ŅȵŗĖŲ”¢²ĻĖ攢ČĖŌģÄĢÓĶ³ä·ÖĖ®½ā¾łæɵƵ½°±»łĖį | |
| B£® | ”°¹ā»ÆѧŃĢĪķ”±”¢”°³ōŃõæÕ¶“”±”¢”°ĪĀŹŅŠ§Ó¦”°”¢”°ĖįÓź”±µÄŠĪ³É¶¼ÓėµŖŃõ»ÆŗĻĪļÓŠ¹Ų | |
| C£® | ĢģČ»Ęų”¢ÕÓĘų”¢¾Ę¾«”¢Ė®ĆŗĘų¾łŹōÓŚæÉŌŁÉśÄÜŌ“ | |
| D£® | ÓĆĶŃĮņ“¦ĄķµÄĆŗ“śĢęŌĆŗ×÷Č¼ĮĻ²»ÄÜÓŠŠ§¼õÉŁæÕĘųÖŠCO2ŗ¬Įæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | HClµÄµē×ÓŹ½ | B£® | Cl-µÄ½į¹¹Ź¾Ņā  | ||
| C£® | CO2µÄµē×ÓŹ½  | D£® | ÖŹĮæŹżĪŖ37µÄĀČŌ×Ó ${\;}_{37}^{17}$Cl |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| »ģŗĻĪļ | ŹŌ¼Į | ·ÖĄė·½·Ø | |
| A | ±½£Ø±½·Ó£© | äåĖ® | ¹żĀĖ |
| B | ŅŅĶé£ØŅŅĻ©£© | ĒāĘų | ¼ÓČČ |
| C | ŅŅ“¼£ØĖ®£© | ŠĀÖʵÄŃõ»ÆøĘ | ÕōĮó |
| D | ±½£Ø¼×±½£© | ÕōĮóĖ® | ·ÖŅŗ |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŗ¬Į×Ļ“ŅĀ·Ū | B£® | ĒāŃõČ¼ĮĻµē³Ų | C£® | ·śĄū°ŗ | D£® | ŗ¬¹Æµē³Ų |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā


 £©£¬Ć§²ŻĖį·Ö×ÓÖŠÓŠ3øöŹÖŠŌĢ¼Ō×Ó£®
£©£¬Ć§²ŻĖį·Ö×ÓÖŠÓŠ3øöŹÖŠŌĢ¼Ō×Ó£®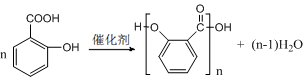 £®
£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com