
【题目】一定质量的某铁的氧化物FexOy,与足量的4 mol·L-1硝酸溶液充分反应,消耗硝酸溶液700 mL,生成2.24 L NO(标准状况)。则该铁的氧化物的化学式为( )
A.FeOB.Fe2O3C.Fe3O4D.Fe4O5
科目:高中化学 来源: 题型:
【题目】2019年,大连化物所研究人员在乙酰酮修饰锰氧化物L酸催化胺选择氧化研究方面取得新的进展(如图甲所示),相关文章发表在《自然通讯》上。请回答下列问题:
(1)基态Mn原子的价电子排布图为________________,其中最外层电子的电子云轮廓图的形状为________________。
(2)图甲中涉及的非金属元素(除H外)第一电离能由小到大的顺序是________________(用元素符号表示,下同),电负性由小到大的顺序是________________。
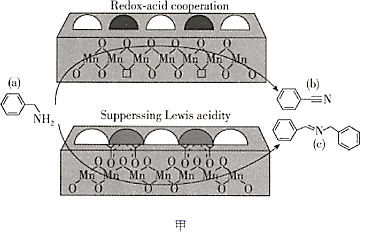
(3)物质a可与水互溶,主要原因是________________。
(4)物质b中碳原子的轨道杂化方式有________________,1 mol物质c中含有σ键的数目为________________。
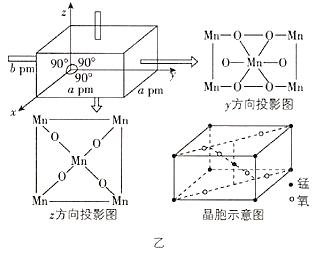
(5)该锰氧化物的晶胞结构如图乙所示,该锰氧化物的化学式为________________,该晶体中Mn的配位数是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要0.1mol·L-1NaOH溶液450mL和0.5mol·L-1硫酸溶液500mL。根据这两种溶液的配制情况回答下列问题:
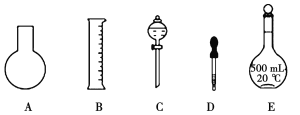
(1)如图所示的仪器中配制溶液肯定不需要的是__________(填序号),配制上述溶液还需用到的玻璃仪器是__________(填仪器名称)。
(2)配制0.1mol·L-1NaOH溶液操作步骤如下:
①把称量好的NaOH`固体放入小烧杯中,加适量蒸馏水溶解;
②把①所得溶液冷却至室温,再小心转入一定容积的容量瓶中;
③继续向容量瓶中加蒸馏水至液面距刻度线1~2cm处,改用胶头滴管小心滴加蒸馏水至溶液凹液面与刻度线相切;
④用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心转入容量瓶,并轻轻摇匀;
⑤将容量瓶瓶塞塞紧,充分摇匀。
操作步骤的正确顺序为__________(填序号)。
(3)根据计算用托盘天平称取NaOH的质量为__________g。在实验中其他操作均正确,若容量瓶用蒸馏水洗涤后未干燥,则所得溶液浓度______________0.10mol·L-1(填“大于”“等于”或“小于”,下同)。若还未等溶液冷却就定容了,则所得溶液浓度__________0.10mol·L-1。
(4)根据计算得知,所需质量分数为98%、密度为1.84g·cm-3的浓硫酸的体积为__________mL(计算结果保留一位小数)。如果实验室有10mL、15mL、20mL、50mL的量筒,应选用__________mL的量筒最好。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学校化学学习小组为探究二氧化氮的性质,按下图所示装置进行实验。

(1)装置甲中盛放浓硝酸的仪器A的名称是______,该装置中发生反应的化学方程式为________________________。
(2) 装置丙中的试管内发生反应的离子方程式为:_______________________。
(3)为了探究NO的还原性,可以在装置丁的导气管C中通入一种气体,通入的这种气体的名称是________。
(4)取下装置丙中的试管D,在其中滴加FeSO4溶液,溶液变为________色,为了证明铁元素在该反应中的产物,可以再在溶液中滴加KSCN溶液,溶液变为________色。
(5)硝酸厂常用催化还原方法处理尾气。CH4在催化条件下可以将NO2还原为N2。
已知:CH4(g)+2O2(g)===CO2(g)+2H2O(g)ΔH=-889.6 kJ·mol-1①
N2(g)+2O2(g)===2NO2(g)ΔH=+67.7 kJ·mol-1②
则CH4还原NO2生成水蒸气和氮气的热化学方程式是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列选项中离子能大量共存的是( )
(1)与铝粉反应放出H2的无色溶液:NO3-、Al3+、Na+、SO42-
(2)含有大量NO3-的溶液:H+、Fe2+、Cl-、SO42-
(3)中性溶液:Fe3+、Al3+、NO3-、SO42-
(4)使pH试纸显蓝色的溶液:Cu2+、NO3-、Fe3+、SO42-
(5)含有大量Fe3+的溶液:Na+、SCN-、Cl-、I-
(6)常温下![]() =1×10-12的溶液:K+、AlO2-、CO32-、Na+
=1×10-12的溶液:K+、AlO2-、CO32-、Na+
(7)c(H+)=0.1 mol·L-1的溶液:Na+、NH4+、SO42-、S2O32-
A.(3)(6)B.(2)(3)(6)C.(6)D.(2)(6)(7)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】国际计量大会第26届会议新修订了阿伏加徳罗常数(NA=6.02214076×1023mol-1),并于2019年5月20日正式生效。下列说法中正确的是
A.12g金刚石中含有化学键的数目为4NA
B.将7.1g Cl2溶于水制成饱和氯水,溶液中Cl-、ClO-和HC1O的微粒数之和为0.1NA
C.标准状况下,11.2L NO和11.2L O2混合后,气体的分子总数为0.75NA
D.20g的D2O中含有的质子数为10NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁一空气电池是一种能被水激活的一次性储备电池,原理如图所示。下列说法错误的是

A. 放电时,外电路电子由镁电极流向多孔碳材料电极
B. 放电时,正极的电极反应式为O2+ 4e—+ 2H2O =4OH
C. 理论上,外电路中流过2 mol电子时,负极质量增加58 g
D. 电池反应产物Mg(OH)2经过灼烧与还原可制成镁锭循环利用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为研究沉淀的生成及其转化,某小组进行如图实验。关于该实验的分析不正确的是
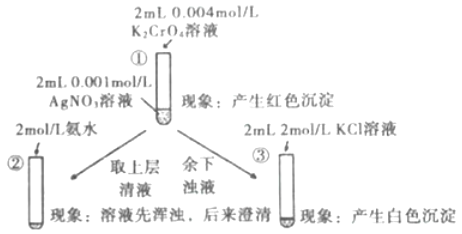
A.①浊液中存在平衡:Ag2CrO4(s)2Ag+(aq)+CrO42-(aq)
B.②中溶液变澄清的原因:AgOH+2NH3·H2O=[Ag(NH3)2]OH+2H2O
C.③中颜色变化说明有AgCl生成
D.该实验可以证明AgCl比Ag2CrO4更难溶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电解质溶液的说法正确的是
A.常温下,0.1 mol/L Na2S溶液中存在:c(OH﹣)=c(H+)+c(HS﹣)+c(H2S)
B.0.1mol/L NaHCO3溶液与0.1mol/L NaOH溶液等体积混合,所得溶液中:C(Na+)>c(CO32-)>c(HCO3- )>c(OH-) >c(H+)
C.pH相同的①CH3COONa②NaHCO3③NaClO三种溶液的c(Na+):①>②>③
D.向0.1 mol·L-1的氨水中加入少量硫酸铵固体,则溶液中c(OH﹣)/c(NH3·H2O)增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com