
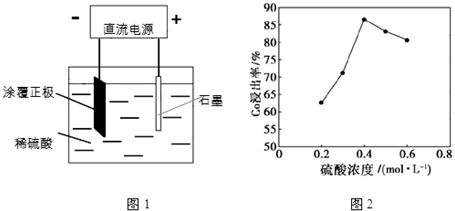
分析 (1)①阴离子氢氧根在阳极放电,生成氧气;
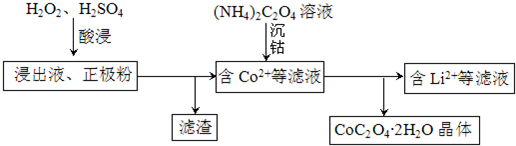
②如图2所示.当c(H2SO4)>0.4mol•L-1时,参与放电的H+增多(或有利于H+放电),所以钴的浸出率下降;
(2)①“酸浸”过程中正极粉发生氧化还原反应,LiCoO2氧化生成Co2+和O2,方程式为2LiCoO2+H2O2+3H2SO4═Li2SO4+2CoSO4+O2↑+4H2O;该步骤一般在80℃以下进行,温度太高,双氧水会受热分解;
②(NH4)2C2O4溶液呈弱酸性,故
a.根据离子浓度大小分析;
b.由电荷守恒分析;
c.由物料守恒分析.
解答 解:(1)①阴离子氢氧根在阳极放电,生成氧气,4OH--4e-═O2↑+2H2O,故答案为:4OH--4e-═O2↑+2H2O;
②如图2所示.当c(H2SO4)>0.4mol•L-1时,参与放电的H+增多(或有利于H+放电),所以钴的浸出率下降,
故答案为:H+与LiCoO2在阴极的还原反应相互竞争,当c(H+)增大时,参与放电的H+增多(或有利于H+放电),所以钴的浸出率下降;
(2)①“酸浸”过程中正极粉发生氧化还原反应,LiCoO2氧化生成Co2+和O2,方程式为2LiCoO2+H2O2+3H2SO4═Li2SO4+2CoSO4+O2↑+4H2O;该步骤一般在80℃以下进行,温度太高,双氧水会受热分解;
故答案为:2LiCoO2+H2O2+3H2SO4═Li2SO4+2CoSO4+O2↑+4H2O;防止H2O2剧烈分解;
②(NH4)2C2O4溶液呈弱酸性,故
a.由离子浓度大小关系,知c (NH4+)>c(C2O42-)>c (H+)>c (OH-),故a正确;
b.由电荷守恒,可知c (H+)+c (NH4+)=c (OH-)+c(HC2O4-)+2c(C2O42-),故b错误;
c.由物料守恒,可知c (NH4+)+c (NH3•H2O)=2[c(C2O42-)+c(HC2O4-)+c(H2C2O4)],故c正确;
故答案为:ac.
点评 本题为生产流程题,涉及金属的回收、环境保护、氧化还原反应、物质的分离提纯和除杂等问题,题目较为综合,做题时注意仔细审题,从题目中获取关键信息,难度中等,难点是电极反应式的书写.


科目:高中化学 来源: 题型:选择题
| A. | 两个相邻同系物的分子量数值一定相差14 | |
| B. | 具有相同通式的有机物不一定互为同系物 | |
| C. | 分子为C3H8与C6H14的两种有机物一定互为同系物 | |
| D. | 分子组成相差一个或几个CH2原子团的化合物必定互为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 13C与15N有相同的中子数 | |
| B. | 1H2O与2H2O互为同素异形体 | |
| C. | 14C与14N互为同位素 | |
| D. | CH3-CH2OH和CH3-O-CH3互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 物质 | 杂质 | 除杂试剂或操作方法 | |
| A. | FeSO4 | CuSO4 | 加入过量铁粉,过滤 |
| B. | NaNO3 | CaCO3 | 溶解、过滤、蒸发 |
| C. | NaCl溶液 | I2 | 加酒精,萃取分液 |
| D. | KNO3溶液 | AgNO3 | 加入NaCl溶液,过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com