
| 选项 | 实验操作 | 现象 | 结论 |
| A | 等体积pH=2的HX和HY两种酸分别与足量的铁反应,用排水法收集气体 | HX放出的氢气多且反应速率快 | HX酸性比HY强 |
| B | 向某溶液中滴入氯化钡溶液和稀硝酸 | 生成白色沉淀 | 说明原溶液含Ba2+ |
| C | 在稀硫酸中加入铜,再加入硝酸钠固体 | 开始无现象,后铜逐步溶解,溶液变蓝,有气泡产生 | 硝酸钠可以加快铜与稀硫酸的反应速率 |
| D | 将一铝箔放在酒精灯外焰上灼烧 | 铝箔熔化但不滴落 | 铝箔表面生成致密的Al2O3薄膜,且Al2O3熔点高于Al |
| A. | A | B. | B | C. | C | D. | D |
分析 A.等pH时HX放出氢气多,可知其浓度大;
B.生成的白色沉淀可能为氯化银或硫酸钡,原溶液中可能含有硫酸根离子或银离子,无法确定是否含有钡离子;
C.酸性条件下,Cu、硝酸根离子发生氧化还原反应;
D.氧化铝的熔点高,包裹在Al的外面.
解答 解:A.等pH时HX放出氢气多,可知其浓度大,则HX的酸性弱,故A错误;
B.向某溶液中滴入氯化钡溶液和稀硝酸,生成的白色沉淀可能为硫酸钡或AgCl,原溶液中可能含有银离子和硫酸根等离子,无法确定是否含有Ba2+,故B错误;
C.酸性条件下,Cu、硝酸根离子发生氧化还原反应,则结论不合理,故C错误;
D.氧化铝的熔点高,包裹在Al的外面,则铝箔熔化但不滴落,故D正确;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握酸性比较、离子检验、氧化还原反应、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | υ(NH3)=0.04mol•L-1•min-1 | B. | υ(H2)=0.06mol•L-1•min-1 | ||
| C. | υ(N2)=0.06mol•L-1•min-1 | D. | υ(N2)=0.03mol•L-1•min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
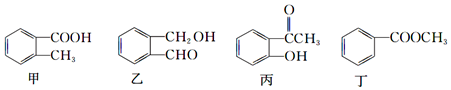
| A. | 甲:①②③④⑥⑦ | B. | 乙:①②③⑤⑥⑦ | C. | 丙:①②③④⑤⑥⑦ | D. | 丁:②③④⑤⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| ① | ② | ||||||
| ③ | ④ | ⑤ | ⑥ | ⑦ | |||
| ⑧ | ⑨ |
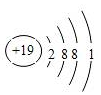
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验目的 | 实验步骤和装置 | |
| A | 验证SO2具有漂白性 | 将SO2通入氢氧化钠的酚酞试液中 |
| B | 探究温度对反应速率的影响 | 不同温度下,取0.1 mol/LKI 溶液,向其中先加入淀粉溶液,再加入0.1 mol/L 硫酸,记录溶液出现蓝色的时间 |
| C | 验证牺牲阳极的阴极保护法 | 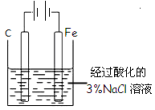 往铁电极附近滴加铁氰化钾溶液 |
| D | 检验蔗糖水解产物具有还原性 | 向蔗糖溶液中加入几滴稀硫酸,水浴加热几分钟,再向其中加入新制的Cu(OH)2,加热3-5min. |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
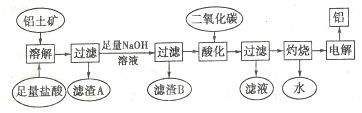
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 改用浓硫酸 | B. | 加热 | ||
| C. | 加入少量CuSO4固体 | D. | 将铁块改成铁粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷和氯气反应属于取代反应 | |
| B. | 乙烯和溴水反应属于取代反应 | |
| C. | 乙醇和酸性高锰酸钾溶液反应属于氧化反应 | |
| D. | 苯燃烧属于氧化反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com