
| t/s | 0 | 500 | 1000 |
| C��H2O��/mol•L-1 | 5.00 | 3.52 | 2.48 |
| C��CO2��/mol•L-1 | 2.50 |
| A�� | ��500s����H2O��g����ʾ�Ļ�ѧ��Ӧ������2.96��10-3mol•L-1•s-1 | |
| B�� | ��500sʱ���ɵ�CH4��Ũ����0.74mol•L-1 | |
| C�� | ��1000sʱ��Ӧ�ﵽƽ�� | |
| D�� | 0-500s��ƽ����Ӧ���ʴ���500��1000s��ƽ����Ӧ���� |
���� A�����ݱ������ݼ�v=$\frac{��c}{��t}$�������500s����H2O��ʾ�Ļ�ѧ��Ӧ���ʣ�
B������H2O��g���ķ�Ӧ���ʼ��������H2O��g�������ʵ������ټ������500sʱ���ɵ�CH4��Ũ�ȣ�
C����ͼ����Ϣ���жϷ�Ӧ�Ƿ��ƽ��״̬��
D���淴Ӧ�Ľ��з�Ӧ���Ũ�ȼ�С����Ӧ���ʱ�С��
��� �⣺A����500s����H2O��ʾ�Ļ�ѧ��Ӧ����Ϊ��v��H2O��=$\frac{��5.00-3.52��mol/L}{500s}$=2.96��10-3mol/��L•s������A��ȷ��
B����500sʱˮ������Ũ�ȱ仯Ϊ����c��H2O��=��5.00-3.52��mol/L=1.48mol/L���ɷ�ӦCO2��g��+2H2O��g��$?_{��}^{����}$CH4��g��+2O2��g������֪�����ɼ�������ʵ���Ũ��Ϊ��c��CH4��=$\frac{1}{2}$��c��H2O��=0.74mol/L����B��ȷ��
C����ͼ����Ϣ���жϷ�Ӧ�Ƿ��ƽ��״̬����C����
D���淴Ӧ�Ľ��з�Ӧ���Ũ�ȼ�С����Ӧ���ʱ�С������0-500s��ƽ����Ӧ���ʴ���500��1000s��ƽ����Ӧ���ʣ���D��ȷ��
��ѡC��
���� ���⿼���˷�Ӧ���ʵļ��㣬��Ŀ�Ѷ��еȣ�ע����ȷ��ѧ��Ӧ�����뻯ѧ�����������ȣ����ջ�ѧ��Ӧ���ʵĸ�������ʽ��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 18 g H2O�к��е�������Ϊ10NA | |
| B�� | 12 g C60�к��е�̼ԭ����Ϊ60NA | |
| C�� | 46 g NO2��N2O4��������к���ԭ������Ϊ3NA | |
| D�� | 1 mol Na������O2��Ӧ������Na2O��Na2O2�Ļ�����ʧȥNA������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 4 | B�� | 5 | C�� | 6 | D�� | 7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 �����жԸ�����������ȷ���ǣ�������
�����жԸ�����������ȷ���ǣ�������| A�� | �����ʿ��Խ�����ȥ��Ӧ | |
| B�� | �����ʿ��Խ���ˮ�ⷴӦ | |
| C�� | 1 mol������������3 mol H2��Ӧ | |
| D�� | �����ʿ��Ժ�Br2����ȡ����Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 3.2g | B�� | 6.4g | C�� | 9.6g | D�� | 12.8g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
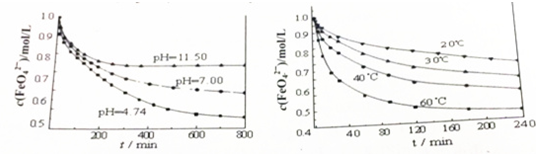
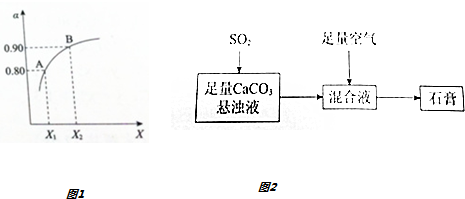
 ������H2O2�ڷ�Ӧʱ��������Ⱦ�����Ϊ��ɫ������������ܵ�����Խ��Խ��Ĺ�ע��
������H2O2�ڷ�Ӧʱ��������Ⱦ�����Ϊ��ɫ������������ܵ�����Խ��Խ��Ĺ�ע��| ʵ���� | ��Ӧ�� | ���� |
| �� | 10mL 2%H2O2��Һ | �� |
| �� | 10mL 5%H2O2��Һ | �� |
| �� | 10mL 5%H2O2��Һ | 1mL 0.1mol•L-1FeCl3��Һ |
| �� | 10mL 5%H2O2��Һ+����HCl��Һ | 1mL 0.1mol•L-1FeCl3��Һ |
| �� | 10mL 5%H2O2��Һ+����NaOH��Һ | 1mL 0.1mol•L-1FeCl3��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������Է�������Ϊ���� | |
| B�� | �������������Է���������ż�� | |
| C�� | �������ĺ������������Է�������Ϊż�� | |
| D�� | �ӡ�ȩ�������ᡢ������Է�������Ϊ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| Ũ��/mol•L-1 | 4��10-6 | 6��10-6 | 2��10-5 | 4��10-5 | 3��10-5 | 2��10-5 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com