
用NA代表阿伏加德罗常数.下列说法正确的是( )
|
| A. | 9g重水(D2O)中所含质子数为0.5×6.02×1023 |
|
| B. | 电解精炼铜时,每转移l mol电子,阳极上溶解的金属必为32g |
|
| C. | 往存在V2O5的密闭容器中加入2molSO2和lmolO2,充分反应后分子总数等于2NA |
|
| D. | VL a mol•L﹣1的氯化铁溶液中,若Fe3+的数目为NA,则Cl﹣的数目大于3NA |
| 阿伏加德罗常数.. | |
| 分析: | A.重水的摩尔质量为20g/mol,重水中含有10个质子,9g重水的物质的量为0.45mol,含有4.5mol质子; B.由于粗铜中含有活泼性较强的铁锌等杂质,电解时铁锌原先放电,所以转移1mol电子,溶解的铜的物质的量小于0.5mol; C.二氧化硫与氧气的反应为可逆反应,反应物不可能完全转化成生成物; D.氯化铁溶液中,铁离子部分水解,铁离子数目小于氯离子. |
| 解答: | 解:A.9g重水的物质的量为0.45mol,0.45mol重水中含有4.5mol质子,含质子数为4.5×6.02×1023,故A错误; B.电解精炼铜时,粗铜中含有杂质铁锌等活泼金属杂质,会比铜先失电子,所以每转移lmol电子,阳极上溶解的金属质量不一定是32g,故B错误; C.往存在V2O5的密闭容器中加入2molSO2和lmolO2,该反应为可逆反应,并不会完全生成三氧化硫,反应后分子的物质的量大于2mol,分子总数大于2NA,故C错误; D.氯化铁溶液中铁离子部分水解,所以溶液中氯离子数目大于铁离子数目的三倍,若Fe3+的数目为NA,则Cl﹣的数目大于3NA,故D正确; 故选D. |
| 点评: | 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,选项C为易错点,注意可逆反应的特点. |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
下列物质分类正确的是
A.SO2、SiO2、CO均为酸性氧化物
B.稀豆浆、硅酸、氯化铁溶液均为胶体
C.烧碱、冰醋酸、四氯化碳均为电解质
D.福尔马林、水玻璃、氨水均为混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
在 1L K2SO4、CuSO4的混合溶液中,c(SO42﹣)=2mol•L﹣1,用石墨作电极电解此溶液,当通电一段时间后(电解完全),两极均收集到22.4L气体(标准状况),原溶液中c(K+)为( )
|
| A. | 0.5 mol•L﹣1 | B. | 1 mol•L﹣1 | C. | 1.5 mol•L﹣1 | D. | 2 mol•L﹣1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
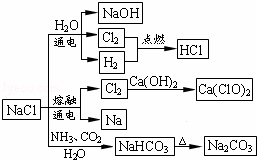
NaCl是一种化工原料,可以制备一系列物质(如图所示).下列说法正确的是( )
|
| A. | 石灰乳与Cl2的反应中Cl2既是氧化剂,又是还原剂 |
|
| B. | 25℃,NaHCO3在水中的溶解度比Na2CO3的大 |
|
| C. | 常温下干燥Cl2能用钢瓶贮运,所以Cl2不与铁反应 |
|
| D. | 图中所示转化反应都是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
氮是大气中含量丰富的一种元素,氮及其化合物在生产、生活中有着重要作用,减少氮氧化物的排放是环境保护的重要内容之一.请回答下列氮及其化合物的相关问题:
(1)据报道,意大利科学家获得了极具研究价值的N4,其分子结构与白磷分子的正四面体结构相似.已知断裂1mol N﹣N键吸收167kJ热量,生成1mol N≡N键放出942kJ热量,请写出N4气体转变为N2反应的热化学方程式: N4(g)=2N2(g);△H=﹣882kJ/mol .
(2)据报道,NH3可直接用作车用燃料电池,写出该电池的负极反应式: 2NH3+6OH﹣﹣6e﹣=N2+6H2O .
(3)在T1℃时,将5mol N2O5置于10L固定容积的密闭容器中发生下列反应:2N2O5(g)⇌4NO2(g)+O2(g);△H>0.反应至5分钟时各物质的浓度不再发生变化,测得NO2的体积分数为50%.
①求该反应的平衡常数K= 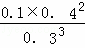 (数字代入式子即可),上述平衡体系中O2的体积分数为 12.5% .
(数字代入式子即可),上述平衡体系中O2的体积分数为 12.5% .
②用O2表示从0~5min内该反应的平均速率υ(O2)= 0.02mol/(L•min) .
③将上述平衡体系的温度降至T2℃,密闭容器内减小的物理量有 AC .
A.压强 B.密度 C.反应速率 D.N2O5的浓度
(4)在恒温恒容的密闭容器中充入NO2,建立如下平衡:2NO2(g)⇌N2O4(g),平衡时N2O4与NO2的物质的量之比为a,其它条件不变的情况下,分别再充入NO2和再充入N2O4,平衡后引起的变化正确的是 B .
A.都引起a减小
B.都引起a增大
C.充入NO2引起a减小,充入N2O4引起a增大
D.充入NO2引起a增大,充入N2O4引起a减小.
查看答案和解析>>
科目:高中化学 来源: 题型:
已知X、Y、Z、W四种短周期元素在周期表中的相对位置如图所示,下列说法正确的是( )
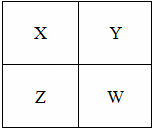
|
| A. | Z元素的原子半径可能比Y元素的小 |
|
| B. | W的原子序数可能是Y的原子序数的2倍 |
|
| C. | W的气态氢化物的稳定性一定比Y的强 |
|
| D. | Z的化学活泼性一定比X强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关电解质溶液中微粒的物质的量浓度关系正确的是( )
|
| A. | pH=3的一元酸和pH=11的一元强碱等体积混合后的溶液中:c(OH﹣)=c(H+) |
|
| B. | 在0.1 mol•L﹣1Na2CO3溶液中:c(OH﹣)﹣c(H+)=c(HCO3﹣)+2c(H2CO3) |
|
| C. | 已知叠氮酸(HN3)与醋酸酸性相近,则在NaN3水溶液中离子浓度大小顺序为:c(Na+)>c(OH¯)>c(N3¯)>c(H+) |
|
| D. | 0.2 mol•L﹣1NaHCO3溶液中加入等体积0.1 mol•L﹣1NaOH溶液:c(CO32﹣)>c(HCO3﹣)>c(OH﹣)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.在pH=1的溶液中:K+、Na+、SO42–、HCO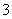
B.在0.1 mol·L-1 Na2CO3溶液中:Al3+、K+、NO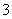 、SO42–
、SO42–
C.在0.1 mol·L-1 FeCl3溶液中:K+、NH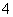 、I-、SCN-
、I-、SCN-
D.在c( H+)/c(OH-)=10-12的溶液中:K+、Na+、ClO-、NO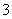
查看答案和解析>>
科目:高中化学 来源: 题型:
在下列变化①大气固氮②炽热的碳和浓HNO3反应③实验室制取氨气中,按氮元素被氧化、被还原、既不被氧化又不被还原的顺序排列,正确的是( )
A.①②③ B.②①③
C.③②① D.③①②
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com