
【题目】F和F—两种粒子中,不相同的是
①核内质子数 ②核外电子数 ③最外层电子数 ④核外电子层数
A. ②③B. ①②C. ③④D. ②③④
科目:高中化学 来源: 题型:
【题目】如图所示,是在其他条件一定时,反应2A+B2C△H<0,A的最大转化率与温度关系曲线,下列叙述正确的是( ) 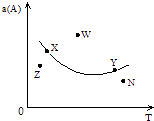
A.X或Y两点相应,V(正)>V(逆)
B.Z、N两点表示未达平衡状态,且都是V(正)>V(逆)
C.W点表示非平衡状态,V(正)>V(逆)
D.相应反应速率大小的点:W>Y>N
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能通过置换反应得到金属铁的是
A. Na与FeSO4溶液常温混合 B. CO通过灼热的Fe2O3
C. H2通入FeSO4溶液 D. Al和Fe3O4混合加热至高温
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期主族元素W、X、Y、Z的原子序数依次增大,W、X的简单离子具有相同电子层结构,X的原子半径是短周期主族元素原子中最大的,W与Y同族,Z与X形成的离子化合物的水溶液呈中性.下列说法正确的是( )
A.简单离子半径:W<X<Z
B.W与X形成的化合物溶于水后溶液呈碱性
C.气态氢化物的热稳定性:W<Y
D.最高价氧化物的水化物的酸性:Y>Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用可溶性钡盐检验SO42-离子的存在时,先在待测溶液中加入盐酸,其作用是
A. 形成较多的白色沉淀 B. 排除SO42-以外的其它阴离子及Ag+的干扰
C. 形成的沉淀纯度更高 D. 排除Ba2+以外的其它阳离子的干扰
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解饱和NaCl溶液是化学工业的重要反应之一。20℃时,饱和NaCl溶液的密度为ρg·cm-3,物质的量浓度为cmol·L-1,则下列说法中不正确的是( )
A. 温度高于20℃时,饱和NaCl溶液的密度大于ρg·cm-3
B. 此溶液中NaCl的质量分数为58.5c/(1000ρ)%
C. 20℃时,浓度小于c mol·L-1的NaCl溶液是不饱和溶液
D. 20℃时,饱和NaCl溶液的溶解度S=5850c/(1000ρ-58.5c)g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是: ①CH3OH(g)+H2O(g)═CO2(g)+3H2(g)△H=+49.0kJmol﹣1
②CH3OH(g)+ ![]() O2(g)═CO2(g)+2H2(g)△H=﹣192.9kJmol﹣1
O2(g)═CO2(g)+2H2(g)△H=﹣192.9kJmol﹣1
下列说法正确的是( )
A.CH3OH的燃烧热为192.9 kJmol﹣1
B.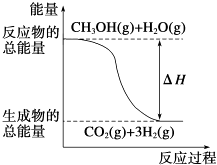 反应①中的能量变化如图所示
反应①中的能量变化如图所示
C.CH3OH转变成H2的过程一定要吸收能量
D.根据②推知反应CH3OH(l)+ ![]() O2(g)═CO2(g)+2H2(g)的△H>﹣192.9 kJmol﹣1
O2(g)═CO2(g)+2H2(g)的△H>﹣192.9 kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有200mL MgCl2和 AlCl3的混合溶液,其中c(Mg2+)=0.2mol/L,c(Cl﹣)=1.3mol/L,要使Mg2+全部转化为沉淀分离出来,至少需要2 mol/L NaOH 溶液的体积是( )
A. 40mL B. 72 mL C. 80 mL D. 160mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验测得1mol H2与1mol Cl2反应生成2mol HCl时,放出184.6kJ的热量,其理论分析数据与实验数据略有差异,如图表示上述反应能量变化的理论分析示意图:
(1)化学键断裂需要(填“释放”或“吸收”)能量;
(2)图中表示了吸收和释放的能量,其中释放的能量共kJ;
(3)该反应的反应物的总能量(填“大于”、“等于”或“小于”)反应产物的能量,所以该反应是(填“放热”或“吸热”)反应;
(4)用图示数据计算其反应热,写出该反应的热化学方程式 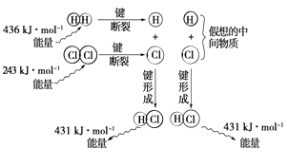
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com