
分析 ①恒温恒压时,向容器中充入0.5mol的He,总体积增大,反应物浓度减小;
②恒温恒容时,加入0.3mol的CO,CO为反应物,且浓度增大.
解答 解:①恒温恒压时,向容器中充入0.5mol的He,总体积增大,反应物浓度减小,则反应速率减慢,
故答案为:减慢;恒温恒压时充入He,体系体积增大,反应物浓度减小,反应速率减慢;
②恒温恒容时,加入0.3mol的CO,CO为反应物,且浓度增大,则反应速率加快,故答案为:加快;反应物CO的浓度增大,反应速率加快.
点评 本题考查反应热计算及影响反应速率的因素,为高频考点,侧重于双基的考查,把握影响反应速率的因素为解答的关键,注重化学反应原理的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
 将一定质量的镁、铝合金投入100mL一定物质的量浓度的盐酸中,使合金全部溶解.向所得溶液中滴加5mol/L NaOH溶液至过量,生成沉淀的质量与加入的NaOH溶液体积的关系如图曲线所示.则盐酸的物质的量浓度为( )
将一定质量的镁、铝合金投入100mL一定物质的量浓度的盐酸中,使合金全部溶解.向所得溶液中滴加5mol/L NaOH溶液至过量,生成沉淀的质量与加入的NaOH溶液体积的关系如图曲线所示.则盐酸的物质的量浓度为( )| A. | 1mol/L | B. | 8mol/L | C. | 10mol/L | D. | 12mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
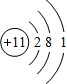 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,2.24LCH4含有的H原子数为0.1NA | |
| B. | 常温常压下,NA个CO2分子占有的体积为22.4L | |
| C. | 1 mol•L-1A1Cl3溶液中含有的Cl-数目为3NA | |
| D. | 2.4g金属镁变为镁离子时失去的电子数为0.2 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe分别与氯气和稀盐酸反应所得氯化物相同 | |
| B. | Al、Fe、Cu三者的单质放置在空气中均只生成氧化物 | |
| C. | Al、Fe、Cu三者对应的氧化物均为碱性氧化物 | |
| D. | C、P、S、Cl的最高价氧化物对应水化物的酸性逐渐增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向某溶液中滴加KSCN溶液不变色,滴加氯水后溶液显红色,原溶液中一定含Fe2+ | |
| B. | 用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液中一定不含K+ | |
| C. | 向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀生成,该溶液一定含有SO42- | |
| D. | 向某盐溶液中加入稀盐酸,产生的气体能使澄清石灰水变浑浊,该溶液一定是碳酸盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 某酸性溶液中,HCO${\;}_{3}^{-}$、CO${\;}_{3}^{2-}$、Na+可大量共存 | |
| B. | NA表示阿伏加德罗常数,则常温常压下,3.0g乙烷中含有的碳氢键数为0.6NA | |
| C. | 实验室中,常用玻璃瓶盛放氢氟酸 | |
| D. | 用饱和NaHCO3溶液可除去CO2中的HCl气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X的值为1 | |
| B. | M的平均反应速率为0.15 mol•L-1•min-1 | |
| C. | M的转化率为60% | |
| D. | 平衡时P的浓度为0.25 mol•L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com