
在一定条件下进行如下反应: aX(g)+bY(g) ![]() cZ(g)下图是不同温度下反应达到平衡时,反应混合物中Z的体积分数和压强关系示意图。
cZ(g)下图是不同温度下反应达到平衡时,反应混合物中Z的体积分数和压强关系示意图。
①写出该反应的化学平衡常数表达式:K= 。随着温度的升高,K值 (填“增大”、“减少”、或“不变”)。当反应物起始浓度相同时,平衡常数K值越大,表明 (填序号)
A.X的转化率越高 B.反应进行得越完全
C.达到平衡时X的浓度越大 D.化学反应速率越快
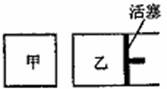
②如下图所示,相同温度下,在甲、乙两容器中各投入1molX、2molY和适量催化剂,甲、乙两容器的初始体积均为1L。甲、乙容器达到平衡所用时间:甲 乙(填“>”、“<”或“=”,下同),平衡时X和Y的转化率:甲 乙。
 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案科目:高中化学 来源: 题型:

| c2(NH3) |
| c(N2)?c3(H2) |
| c2(NH3) |
| c(N2)?c3(H2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
 在一密闭容器中充入X和Y,在一定条件下进行如下反应:aX(g)+bY(g)
在一密闭容器中充入X和Y,在一定条件下进行如下反应:aX(g)+bY(g)  cZ(g)+dW(s),如图I是不同温度下反应达到平衡时,反应混合物中Z的体积分数和压强关系的示意图,下列说法中正确的是( )
cZ(g)+dW(s),如图I是不同温度下反应达到平衡时,反应混合物中Z的体积分数和压强关系的示意图,下列说法中正确的是( )查看答案和解析>>
科目:高中化学 来源: 题型:
 (2008?南京二模)(1)土壤的pH一般在4~9之间.土壤中Na2CO3含量较高时,pH可以高达10.5,
(2008?南京二模)(1)土壤的pH一般在4~9之间.土壤中Na2CO3含量较高时,pH可以高达10.5, HCO3-+OH-、HCO3-+H2O
HCO3-+OH-、HCO3-+H2O H2CO3+OH-
H2CO3+OH- HCO3-+OH-、HCO3-+H2O
HCO3-+OH-、HCO3-+H2O H2CO3+OH-
H2CO3+OH-| cc(Z) |
| ca(X)?cb(Y) |
| cc(Z) |
| ca(X)?cb(Y) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| O | 2- 3 |
| O | - 3 |
| H | + 4 |

查看答案和解析>>
科目:高中化学 来源: 题型:
| 试验编号 | ① | ② | ③ |
| 所加0.4moL/LH2SO4 溶液的体积 | 30mL | ||
| 所加0.2 moL/LCuSO4溶液的体积 | 0 | 0.5mL | 5mL |
| 所加蒸馏水的体积 | 5mL | ||
| 探究硫酸铜对硫酸与锌反应速率的影响 | . | ||
| 设计实验室应注意的问题 | |||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com