
下列有关碱金属的说法正确的是
A、碱金属元素随原子序数的递增原子半径逐渐减小
B、碱金属元素随原子序数的递增离子氧化性逐渐减弱
C、碱金属元素的单质在氧气点燃都生成过氧化物
D、碱金属元素随原子序数的递增最高价氧化物对应的水化物碱性逐渐减弱
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl4SOCl2。电池的总反应可表示为4Li+2SOCl2===4LiCl+S+SO2↑。
请回答下列问题:
(1)电池的负极材料为__________,发生的电极反应为_______________________。
(2)电池正极发生的电极反应为_____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列鉴别方法可行的是
A.用氨水鉴别Al3+、Mg2+和Ag+ B.用盐酸酸化的BaCl2溶液鉴别Cl-、SO 和CO
和CO
C.用溴水鉴别CH4和C2H4 D.用KMnO4酸性溶液鉴别CH3CH2OH和CH3CHO
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,在一密闭容器中将1.0 mol/L N2与3.0 mol/L H2合成氨,反应到2s时测得
NH3的浓度为0.8 mol/L,用N2浓度的变化量来表示该反应速率时,该反应的反应速率为
A、0.2 mol/(L·s) B、0.4 mol/(L·s) C、0.6 mol/(L·s) D、0.8 mol/(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E是原子序数由小到大排列的五种短周期元素,其中B、C、D的原子序数之和为31,A是元素周期表中原子半径最小的元素,B、C左右相邻,C、D位于同主族.
(1)E元素原子的结构示意图为: ,写出一个能证明D、E两元素非金属性强弱的反应方程式: .
(2)用电子式表示A与B形成含10个电子的分子的过程 ,其中含有的化学键为 (填“极性键”“非极性键”“离子键”).
(3)A、B、C、D四种元素中的三种能组成一种强酸,该强酸的稀溶液能与铜反应,其中起酸性作用的酸占消耗酸总物质的量的百分比是 .
(4)由A、B、C、D四种元素组成的一种离子化合物X.
①已知1mol X能与足量NaOH浓溶液反应生成标准状况下44.8L气体.写出加热条件下X与NaOH浓溶液反应的离子方程式: .
②又知X既能与E和A形成的化合物反应,又能与E形成的单质的水溶液起反应,写出X的化学式: .
(5)A、B、C、D和Fe五种元素组成相对分子质量为392的化合物Y,1mol Y中含有6mol结晶水.对化合物Y进行如下实验:
a.取Y的 溶液加入过量浓NaOH溶液并加热,产生白色沉淀和无色有刺激性气味的气体.过一段时间白色沉淀变为灰绿色,最终变为红褐色.
b.另取Y的溶液,加入过量BaCl2溶液产生白色沉淀,加盐酸沉淀不溶解.
①Y的化学式为 .
②写出Y与足量Ba(OH)2溶液反应的离子方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中正确的是 ( )。
A.NH3、CO、CO2都是极性分子
B.CH4、CCl4都是含有极性键的非极性分子
C.HF、HCl、HBr、HI的稳定性依次增强
D.CS2、H2O、C2H2都是直线形分子
查看答案和解析>>
科目:高中化学 来源: 题型:
Fe、C、N、O、H可以组成多种物质。回答以下问题:
(1)基态铁原子中,未成对电子数有 个。
(2)铁单质在一定条件下可与CO反应生成配位化合物——羰基
铁[Fe(CO)5],其结构如右图。已知CO分子与N2分子结构相
似,分子中C、O原子均能提供孤电子对形成配位键。
①CO分子中σ键与π键数目之比为 ;
②从电负性角度分析,Fe(CO)5中与Fe形成配位键的是 (填“碳”或“氧”)原子。
 ③与羰基铁分子的极性相似的分子是 。
③与羰基铁分子的极性相似的分子是 。
A.SO2 B.CS2 C.BF3 D.PCl3
(3)CH4、H2O分子的键角分别为a、b。则a b
(填>、=或<),原因是 。
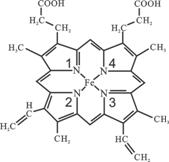
(4)血红素分子结构如右图所示。
①血红素分子间存在的作用力有 (填名称);
②与Fe通过配位键结合的氮原子的编号是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
化学工艺中倡导无污染的绿色化学是一场新的技术革命。若使用单质铜制硝酸铜,下列方案中,耗用原料最经济,而且对环境几乎没有污染的是( )
A.Cu和稀硝酸反应制Cu(NO3)2
B、Cu和浓硝酸反应制Cu(NO3)2
C、铜在空气中受热转化为CuO,再溶于稀硝酸制Cu(NO3)2
D、铜在氧气中受热转化为CuO,再溶于浓硝酸制Cu(NO3)2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com