
难挥发性二硫化钽(TaS2 )可采用如下装置提纯。将不纯的TaS2 粉末装入石英管一端,抽真空后引入适量碘并封管,置于加热炉中。反应如下: TaS2(g)+ 2I2(g) TaI4(g) + S2(g),下列说法错误的是
TaI4(g) + S2(g),下列说法错误的是
| A.在不同温度区域,TaI4 的量不同 |
| B.在提纯过程中,S2 的量不断增多 |
| C.该反应的平衡常数不随TaI4 和S2 的浓度增大而增大 |
| D.在提纯过程中,I2 的作用是将TaS2 从高温区转移到低温区 |
科目:高中化学 来源: 题型:单选题
下列有关说法正确的是
| A.恒温时,向水中加入少量固体硫酸氢钠,c(H+)增大,水的离子积常数Kw不变 |
| B.0.1mol/LCH3COONa溶液中:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
C.对于N2(g)+3H2(g) 2NH3(g),其他条件不变,充入N2,正反应速率增大,逆反应速率减小 2NH3(g),其他条件不变,充入N2,正反应速率增大,逆反应速率减小 |
| D.在硫酸钡悬浊液中加入足量饱和Na2CO3溶液,振荡、过滤、洗涤,沉淀中加入盐酸有气体产生,说明Ksp(BaSO4)>Ksp(BaCO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关说法正确的是
| A.准确称取0.4000 g NaOH固体可配成100 mL 0.1000 mol·L-1的NaOH标准溶液 |
| B.催化剂可以加快化学反应速率但不能改变化学反应的焓变 |
| C.100 mL pH=3的HA和HB分别与足量的锌反应,HB放出的氢气多,说明HB酸性比HA弱 |
D.对于反应2SO2(g)+O2(g)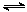 2SO3(g),压缩气体体积使压强增大(其他条件不变),则SO2的转化率增大,平衡常数K也增大 2SO3(g),压缩气体体积使压强增大(其他条件不变),则SO2的转化率增大,平衡常数K也增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列过程属于熵(S)增加的是 ( )
| A.一定条件下,水由气态变成液态 | B.高温高压条件下使石墨转变成金刚石 |
| C.4NO2(g)+O2(g)=2N2O5 (g) | D.CaCO3(s)=CaO(s)+CO2(g) |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某同学用以下实验用品设计验证碘化钾与氯化铁反应的限度:0.1mol·L–1KI溶液、0.1mol·L–1FeCl3溶液、CCl4、淀粉溶液、KSCN溶液、试管、胶头滴管等。该同学设计的实验方案如图:
根据以上实验方案判断下列说法不正确的是
| A.试剂a是0.1mol·L–1KI溶液 |
| B.试剂d是KSCN溶液 |
| C.说明该反应已经发生的理由是③的下层呈紫色 |
| D.说明该反应是有限度的实验现象是④的上层溶液出现血红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在密闭容器中进行反应CH4(g)+H2O(g) CO(g)+3H2(g) ΔH>0,测得c(CH4)随反应时间(t)的变化如图所示。下列判断不正确的是 ( )。
CO(g)+3H2(g) ΔH>0,测得c(CH4)随反应时间(t)的变化如图所示。下列判断不正确的是 ( )。
| A.10 min时,改变的外界条件可能是升高温度 |
| B.0~10 min内,v(H2)=0.15 mol·L-1·min-1 |
| C.恒温下,缩小容器体积,一段时间内v(逆)>v(正) |
| D.12 min时,反应达平衡的本质原因是气体总质量不再变化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com