
【题目】锰主要用于钢铁工业生产锰合金钢,锰的化合物有+2、+4、+6、+7 等多种变价,以菱锰矿(主要成分为 MnCO3,还含有少量铁、镍、 钴等碳酸盐杂质)为原料经过一系列反应生产金属锰和高锰酸钾的工艺流程如下:

已知 25 ℃时,部分物质的溶度积常数如下:
物质 | Mn(OH)2 | Co(OH)2 | Ni(OH)2 | MnS | CoS | NiS |
Ksp | 2.1×10-13 | 3.0×10-16 | 5.0×10-16 | 1.0×10-11 | 5.0×10-22 | 1.0×10-22 |
(1)酸溶浸过程中,硫酸需稍过量,除保证反应充分进行外,其他作用还有_________(任写一条)。
(2)除杂1过程加入MnO2后,发生氧化还原反应的离子方程式为_________;滤渣2 的主要成分是____________________________。
(3)为加快过滤速度,选择如图抽滤装置完成。下列有关操作和说法正确的是______。

a. 抽滤的本质是加压过滤
b. 抽滤成功的关键在于合理控制水的流速
c. 微粒直径大于滤纸孔径的物质进入吸滤瓶中
(4)电解1过程阳极电极反应式为____________。
(5)H2O2 是一种常用的绿色氧化剂,在平炉反应中不用 H2O2的原因是__________。
(6)“CO2歧化法” 制备 KMnO4是传统工艺,写出该歧化反应的化学方程式_____________。
【答案】 提供除杂 1 时所需要的酸性环境、抑制 Mn2+的水解 MnO2+2Fe2++4H+===Mn2++2Fe3++2H2O CoS 和 NiS b Mn2++2H2O -2e- = MnO2+4H+ 锰的化合物可催化 H2O2 的分解,使消耗的 H2O2 增多 3K2MnO4 +4CO2+2H2O=2KMnO4+MnO2+4KHCO3或3K2MnO4 +2CO2=2KMnO4+MnO2+2K2CO3
【解析】(1)酸溶浸过程中,硫酸需稍过量,除保证反应充分进行外,其他作用还有提供除杂 1 时所需要的酸性环境、抑制 Mn2+的水解;(2)除杂1过程加入MnO2后,将Fe2+氧化为Fe3+,以便于通过调节pH使其转化为沉淀而除去,发生氧化还原反应的离子方程式为MnO2+2Fe2++4H+===Mn2++2Fe3++2H2O;滤渣1为氢氧化铁,再加入硫化铵将钴镍转化为难溶的硫化物,故滤渣2 的主要成分是CoS 和 NiS;(3)a. 抽滤的本质是减压过滤,选项a错误;b. 抽滤成功的关键在于合理控制水的流速,选项b正确;c. 微粒直径小于滤纸孔径的物质进入吸滤瓶中,选项c错误。答案选b;(4)电解1过程阳极Mn2+失电子产生MnO2,电极反应式为Mn2++2H2O -2e- = MnO2+4H+;(5)H2O2 是一种常用的绿色氧化剂,在平炉反应中不用 H2O2的原因是锰的化合物可催化 H2O2 的分解,使消耗的 H2O2 增多;(6)“CO2歧化法” 制备 KMnO4是传统工艺,该歧化反应锰的化合价由+6价变为+7价和+4价,发生的化学方程式为3K2MnO4 +4CO2+2H2O=2KMnO4+MnO2+4KHCO3或3K2MnO4 +2CO2=2KMnO4+MnO2+2K2CO3。


 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案科目:高中化学 来源: 题型:
【题目】将镁铝合金溶于100mL稀硝酸中,产生1.12L NO气体(标准状况),向反应后的溶液中加入NaOH溶液,产生沉淀情况如图所示。下列说法不正确的是

A. 可以求出合金中镁的质量 B. 氢氧化钠溶液浓度为3mol/L
C. 可以求出沉淀的最大质量 D. 不能求出硝酸的物质的量浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关,下列说法不正确的是( )
A.乙醇溶液的浓度越大,对新冠病毒杀灭效果越好
B.氨气易液化,可用来作制冷剂
C.常温下,铝制容器可以用来贮运浓硝酸
D.乙烯可用作水果的催熟剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中,R、W、X、Y、Z为元素周期表中前四周期的部分元素,下列有关叙述正确的是

A. 五种元素中,只有Z为金属元素
B. W位于ⅥA族,有+6、-2两种常见化合价
C. X和Y的最高价氧化物对应水化物都是强酸
D. X、Y、Z的气态氢化物的稳定性:Y>X>Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分离下列三组混合物依次采取的方法正确的是:①碳酸钙和氯化钙的溶液 ②植物油和氯化钠溶液 ③氯化钠溶液和鸡蛋清( )
A.渗析、蒸馏、萃取
B.分液、萃取、蒸馏
C.过滤、分液、聚沉
D.过滤、分液、渗析
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸镧咀嚼片是一种不含钙和铝的磷酸盐结合剂,用于慢性肾衰患者高磷血症的治疗。碳酸镧可由 LaCl3 为原料来制备,整个反应在较低的pH条件下进行,避免生成碱式碳酸镧[La(OH)CO3]。
(1)化学兴趣小组利用下列装置在实验室中用碳酸氢铵制备碳酸镧。

①仪器 X 的名称为________;检验装置甲气密性良好的方法是___________。
②实验中 K1、 K2 打开的先后顺序为________;为保证碳酸镧的纯度,实验过程中需要注意的问题有____________。
(2)碳酸钠或碳酸氢钠与氯化镧反应均可生成碳酸镧。
①为了高磷血症患者的安全,通常选用碳酸氢钠溶液,过程中会发生两个平行反应,其离子方程式为_______和____________。
②选择碳酸氢钠溶液制备碳酸镧的优点是___________(任写一条)。
③T℃时,碳酸镧的溶解度为1.0×10-7 mol·L-1, HCO3-的电离平衡常数为 6.0×10-11。请计算反应 2LaCl3+3NaHCO3![]() La2(CO3)3↓+3NaCl+3HCl 的平衡常数 K=_________。
La2(CO3)3↓+3NaCl+3HCl 的平衡常数 K=_________。
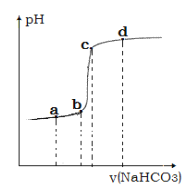
④利用手持技术测定溶液的 pH 从而监控反应过程,得到如图曲线。请说明 bc 段变化的原因__________。
(3)碳酸镧(式量为 458)质量分数的测定:准确称取15.0g产品试样,溶于10.0mL 稀盐酸中,加入 10mLNH3-NH4Cl 缓冲溶液,加入 0.2g 紫脲酸铵混合指示剂,用 0.5 mol·L-1EDTA(Na2H2Y)标准溶液滴定至呈蓝紫色(La3++H2Y2-= LaY-+2H+),消耗 EDTA 溶液 60.00mL。则产品中碳酸镧的质量分数 w=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将BaCl2溶液加入某无色溶液后,生成白色沉淀,再加入稀HNO3 , 则沉淀不溶解,下列说法正确的是( )
A.一定存在Ag+
B.一定存在CO32﹣
C.一定存在SO42﹣
D.以上说法都不对
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图片是立方烷(cunane)的球棍模型,下列有关说法不正确的是( )

A. 其一氯代物只有一种
B. 其二氯代物有三种同分异构体
C. 常温下为气体
D. 它与苯乙烯(C6H5—CH===CH2)互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
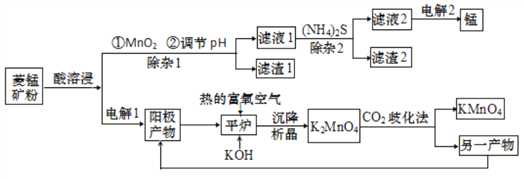
【题目】锰主要用于钢铁工业生产锰合金钢,锰的化合物有+2、+4、+6、+7 等多种变价,以菱锰矿(主要成分为 MnCO3,还含有少量铁、镍、 钴等碳酸盐杂质)为原料经过一系列反应生产金属锰和高锰酸钾的工艺流程如下:
已知 25 ℃时,部分物质的溶度积常数如下:
物质 | Mn(OH)2 | Co(OH)2 | Ni(OH)2 | MnS | CoS | NiS |
Ksp | 2.1×10-13 | 3.0×10-16 | 5.0×10-16 | 1.0×10-11 | 5.0×10-22 | 1.0×10-22 |
(1)酸溶浸过程中,硫酸需稍过量,除保证反应充分进行外,其他作用还有_________(任写一条)。
(2)除杂1过程加入MnO2后,发生氧化还原反应的离子方程式为_________;滤渣2 的主要成分是____________________________。
(3)为加快过滤速度,选择如图抽滤装置完成。下列有关操作和说法正确的是______。
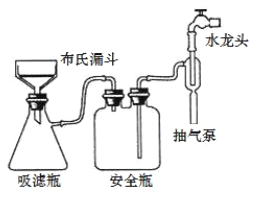
a. 抽滤的本质是加压过滤
b. 抽滤成功的关键在于合理控制水的流速
c. 微粒直径大于滤纸孔径的物质进入吸滤瓶中
(4)电解1过程阳极电极反应式为____________。
(5)H2O2 是一种常用的绿色氧化剂,在平炉反应中不用 H2O2的原因是__________。
(6)“CO2歧化法” 制备 KMnO4是传统工艺,写出该歧化反应的化学方程式_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com