
分析 (1)△H=反应物键能和-生成物键能和;
(2)合成氨是可逆反应,反应物不能完全转化;
(3)v(NH3)=$\frac{\frac{△n}{V}}{△t}$,$\frac{v({N}_{2})}{v(N{H}_{3})}$=$\frac{1}{2}$,据此求算;
(4)化学平衡状态是正逆反应速率相等,各组分浓度保持不变的状态,反应达到最大限度,据此分析.
解答 解:(1)△H=反应物键能和-生成物键能和,反应N2+3H2?2NH3中△H=(946+3×436-6×391)kJ/mol=-92kJ/mol,所以正反应放热,故答案为:放出;92;
(2)合成氨是可逆反应,反应物不能完全转化,故答案为:合成氨是可逆反应,反应物不能完全转化;
(3)v(NH3)=$\frac{\frac{△n}{V}}{△t}$=$\frac{\frac{10mol}{2L}}{10min}$=0.5mol/(L•min),$\frac{v({N}_{2})}{v(N{H}_{3})}$=$\frac{1}{2}$,所以v(N2)=0.25mol/(L•min),故答案为:0.25;
(4)a.正反应速率和逆反应速率相等,说明反应达到平衡状态,正确;
b.正反应速率最大,逆反应速率为0,是指反应开始时的状态,反应没有达到平衡状态,错误;
c.N2的转化率达到最大值,说明反应达到平衡状态,正确;
d.N2和H2的浓度相等,反应不一定达到平衡状态,错误;
e.N2、H2和NH3的体积分数相等,与平衡状态无关,错误;
f.反应达到最大限度,说明反应达到平衡状态,正确;
故答案为:acf.
点评 本题考查了据键能计算焓变、可逆反应的焓变、化学反应速率的计算、化学平衡状态的判断,题目难度不大.


 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 当V<22.4L时,随着CO2气体的通入,溶液中由水电解出的c(H+)逐渐增大 | |
| B. | 当V=22.4L时,所得溶液中存在:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+) | |
| C. | 当22.4L<V<44.8L时,所得溶液中一定存在:c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) | |
| D. | 当V=44.8L时,所得溶液中存在:c(OH-)+c(CO32-)=c(H+)+C(H2CO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
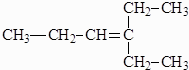 一种有机化合物的结构简式为:
一种有机化合物的结构简式为:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
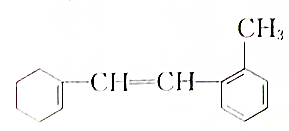 :
:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
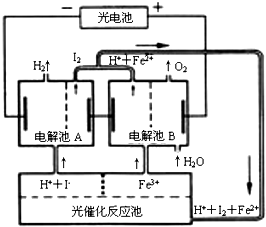
| A. | 外电路中每通过0.2 mol电子,电解池B中就会生成1.12L氧气 | |
| B. | 光催化反应池中离子反应式是:2Fe2++I2$\frac{\underline{\;光照\;}}{\;}$Fe3++2I- | |
| C. | 电解池B中阴极反应式是:Fe3++e-═Fe2+ | |
| D. | 电解池A的阳极反应式是:2I--2e-═I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
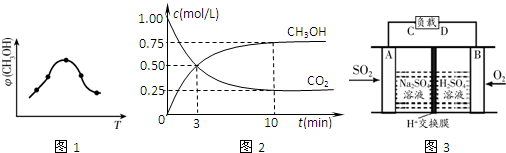
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 方法1 | 用生物质热解气(主要成分CO、CH4、H2)将SO2在高温下还原成单质硫,其部分热化学方程式为: 2CO(g)+SO2(g)=S(g)+2CO2(g)△H=+8.0kJ•mol-1 2H2(g)+SO2(g)=S(g)+2H2O(g)△H=+90.4kJ•mol-1 |
| 方法2 | 用Na2SO3溶液充分吸收SO2得NaHSO3溶液,然后电解该溶液可制得硫酸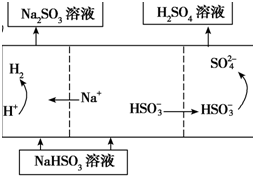 |
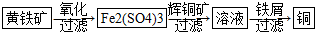
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
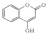 ,常用于制备抗凝血药,可通过下列流程合成:
,常用于制备抗凝血药,可通过下列流程合成: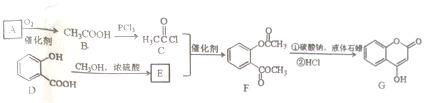
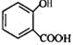 +CH3OH$?_{△}^{浓硫酸}$
+CH3OH$?_{△}^{浓硫酸}$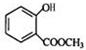 +H2O.
+H2O.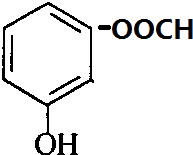 、
、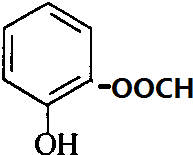 、
、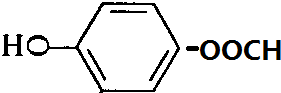 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学将为环境、能源、资源等问题的解决提供有力保障 | |
| B. | 化学正发展成为一门实验与理论互相结合、互相渗透的科学 | |
| C. | 化学是一门具有极强实用性的自然科学 | |
| D. | 化学是一门纯实验的自然科学,实验是探究化学过程的唯一途径 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com