
为了除去食盐中的![]() ,有以下操作步骤:①过滤②加入稍过量的
,有以下操作步骤:①过滤②加入稍过量的![]() 溶液③加稀盐酸调整pH至中性④加入稍过量的
溶液③加稀盐酸调整pH至中性④加入稍过量的![]() 和NaOH溶液,正确的操作顺序是
和NaOH溶液,正确的操作顺序是
[ ]
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案科目:高中化学 来源: 题型:
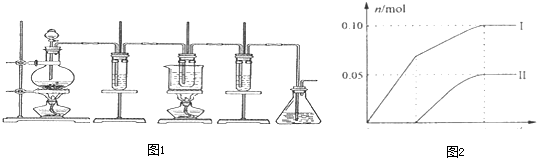
 为验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题:
为验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:名师指点学(化学高三理科) 题型:021
为了除去食盐中的![]() ,有以下操作步骤:①过滤②加入稍过量的
,有以下操作步骤:①过滤②加入稍过量的![]() 溶液③加稀盐酸调整pH至中性④加入稍过量的
溶液③加稀盐酸调整pH至中性④加入稍过量的![]() 和NaOH溶液,正确的操作顺序是
和NaOH溶液,正确的操作顺序是
[ ]
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com