
同温同压下,同体积的N2和SO2分子数之比为 ,物质的量之比为 ,原子总数之比为 ,摩尔质量之比为 ,质量之比为 ,密度之比为 。
1∶1 ,1∶1 ,2∶3 ,7∶16 , 7∶16 ,7∶16 。
【解析】
试题分析:同温同压下,同体积的N2和SO2的物质的量相等,所以分子数也相等,二者的分子数之比为1:1;物质的量之比是1:1;由于N2是双原子分子,而SO2是三原子分子,所以当二者分子数相等时,原子总数之比为就是分子内原子个数之比,是2:3;摩尔质量之比就是二者的相对分子质量之比,为7∶16 ,由于它们的物质的量相等,根据m=n·M可知二者的质量之比7∶16;由于气体的密度ρ=m÷V=M÷Vm,在相同的外界条件下,气体摩尔体积相等,所以气体的密度之比为二者的相对分子质量之比,是7∶16 。
考点:考查阿伏伽德罗定律及推论的应用的知识。


科目:高中化学 来源:2014~2015学年黑龙江省高二上学期期中化学试卷(解析版) 题型:选择题
已知25 ℃、101 kPa条件下:
(1)4Al(s)+3O2(g)===2Al2O3(s) ΔH=-2 834.9 kJ·mol-1
(2)4Al(s)+2O3(g)===2Al2O3(s) ΔH=-3 119.1 kJ·mol-1
由此得出的正确结论是
A.等质量的O2比O3能量低,由O2变O3为吸热反应
B.等质量的O2比O3能量高,由O2变O3为放热反应
C.O3比O2稳定,由O2变O3为吸热反应
D.O2比O3稳定,由O2变O3为放热反应
查看答案和解析>>
科目:高中化学 来源:2014~2015学年江西赣州赣县中学北校区高二9月月考B层化学试卷(解析版) 题型:选择题
一定条件下,可逆反应C(s)+CO2(g) 2CO(g)⊿H=+QkJ/mol,达到平衡状态,现进行如下操作:①升高反应体系的温度;②增加反应物C的用量;③缩小反应体系的体积:④减少体系中CO的量。上述措施中一定能使反应的正反应速率显著加快的 ( )
2CO(g)⊿H=+QkJ/mol,达到平衡状态,现进行如下操作:①升高反应体系的温度;②增加反应物C的用量;③缩小反应体系的体积:④减少体系中CO的量。上述措施中一定能使反应的正反应速率显著加快的 ( )
A、①②③④ B、①③ C、④② D、①③④
查看答案和解析>>
科目:高中化学 来源:2014~2015学年江西赣州赣县中学北校区高二9月月考A层化学试卷(解析版) 题型:选择题
下述实验不能达到预期实验目的的是( )
序号 | 实验内容 | 实验目的 |
A | 将2.5gCuSO4·5H2O溶解在97.5g水中 | 配制质量分数为1.6%的CuSO4溶液 |
B | 向盛有1mL硝酸银溶液的试管中滴加NaCl溶液,至不再有沉淀生成,再向其中滴加Na2S溶液 | 说明一种沉淀能转化为另一种溶解度更小的沉淀 |
C | 室温下,用pH试纸测定浓度为0.1mol·L-1NaClO溶液和0.1mol·L-1CH3COONa溶液的pH | 比较HClO和CH3COOH的酸性强弱 |
D | 室温下,分别向2支试管中加入相同体积、相同浓度的Na2S2O3溶液,再分别加入相同体积不同浓度的稀硫酸 | 研究浓度对反应速率的影响 |
查看答案和解析>>
科目:高中化学 来源:2014~2015学年江西赣州赣县中学北校区高二9月月考A层化学试卷(解析版) 题型:选择题
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是( )
A.氢氧燃料电池的负极反应式:O2 + 2H2O + 4e- = 4OH -
B.铅蓄电池充电时,标示“+”的接线柱连电源的正极,电极反应式为:PbSO4(S) -2e - + 2H2O(l)=PbO2(S) + 4H+(aq)+ SO42-(aq)
C.粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e- = Cu2+
D.钢铁发生电化学腐蚀的正极反应式:Fe-2e - = Fe2+
查看答案和解析>>
科目:高中化学 来源:2014~2015学年江西赣州赣县中学北校区高一9月月考化学试卷(解析版) 题型:选择题
mg某金属M与含n mol HCl的盐酸恰好完全反应,生成MCl2和H2,则该金属的相对原子质量为
A.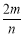 B.
B.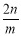 C.
C.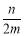 D.
D.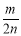
查看答案和解析>>
科目:高中化学 来源:2014~2015学年江西赣州赣县中学北校区高一9月月考化学试卷(解析版) 题型:选择题
过滤后的食盐水仍含有可溶性的CaCl2、MgCl2、Na2SO4等杂质,通过如下几个实验步骤,可制得纯净的食盐水:①加入稍过量的Na2CO3溶液;②加入稍过量的NaOH溶液;③加入稍过量的BaCl2 溶液;④滴入稀盐酸至无气泡产生;⑤过滤 正确的操作顺序( )
A.①②③⑤④ B.③②①⑤④ C.②③①④⑤ D.③⑤②①④
查看答案和解析>>
科目:高中化学 来源:2014~2015学年江西四校9月联考高二化学试卷(解析版) 题型:选择题
已知:2M(g)  N(g);△H <0。现将M和N的混和气体通入体积为1L的恒温密闭容器中,反应体系中物质浓度随时间变化关系如右图所示。下列说法正确的是( )
N(g);△H <0。现将M和N的混和气体通入体积为1L的恒温密闭容器中,反应体系中物质浓度随时间变化关系如右图所示。下列说法正确的是( )
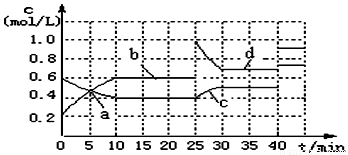
A. a、b、c、d四个点中处于平衡状态的点是a、b d
B. 反应进行至25min时,曲线发生变化的原因是加入了 0.4molN
C. 若调节温度使35min时体系内N的百分含量与15min时相等,应升高温度
D. 若40min后出现如图所示变化,则可能是加入了某种催化剂
查看答案和解析>>
科目:高中化学 来源:2014秋贵州省遵义市高二上学期期中化学(文)试卷(解析版) 题型:选择题
在日常生活中出现了“加碘食盐”、“增铁酱油”、 “富硒茶叶”、“含氟牙膏”等名词,这里的碘、铁、硒、氟应理解为
A.元素 B.单质 C.氧化物 D.分子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com