
| A、在原电池工作时,溶液中的阳离子向负极移动 |
| B、物质发生化学变化时都伴随着能量变化 |
| C、活化分子之间发生的碰撞一定为有效碰撞 |
| D、对有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率加快 |


科目:高中化学 来源: 题型:
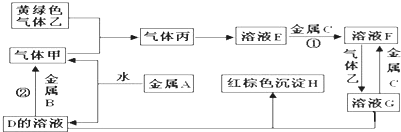
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH=2的醋酸溶液与pH=12的NaOH溶液等体积混合:c(Na+)+c(H+)═c(OH-)+c(CH3COO-) |
| B、Na2CO3溶液中:c(Na+)═2[c(CO32-)+c(HCO3-)+c(H2CO3)] |
| C、NH4HSO4溶液中滴加NaOH至溶液恰好呈中性:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+) |
| D、0.1mol/L pH为4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、小苏打溶液中加入过量的烧碱溶液:HCO3-+OH-═CO32-+H2O |
| B、澄清石灰水中通入过量的CO2:CO2+OH-═HCO3- |
| C、Cl2与水反应生成盐酸和次氯酸Cl2+H2O═H++Cl-+HClO |
| D、向氯化铝溶液中加入足量氨水:Al3++4NH3?H2O═AlO2-+2H2O+4NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、第二周期第IA族 |
| B、第二周期第IIA族 |
| C、第三周期第IA族 |
| D、第三周期第IIA族 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、盐类的水解实质上是破坏了水的电离平衡,促进了水的电离 |
| B、沉淀溶解达到平衡时,如果再加入难溶性的该沉淀物,将促进溶解 |
| C、原电池的正极一定是化学性质较不活泼的金属 |
| D、在溶液中,导电能力强的电解质是强电解质,导电能力弱的电解质是弱电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原混合溶液中c(K+)为3mol?L-1 |
| B、上述电解过程中共转移1mol电子 |
| C、电解得到的Cu的物质的量为0.5mol |
| D、电解后溶液中c(H+)为2mol?L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com