
【题目】下列物质含有离子键的是( )
A.H2O2B.CO2C.NH3D.NaOH
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列反应中,既属于氧化还原反应同时又是吸热反应的是
A.灼热的炭与CO2反应B.甲烷与O2的燃烧反应
C.铝与稀盐酸D.Ba(OH)2·8H2O与NH4Cl反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知C6H14有多种同分异构体,则其同分异构体中沸点最高的分子的一氯取代物的种数(不考虑立体异构)是( )
A. 2 B. 3 C. 4 D. 5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药物比卡鲁安(G)可以通过以下方法合成:
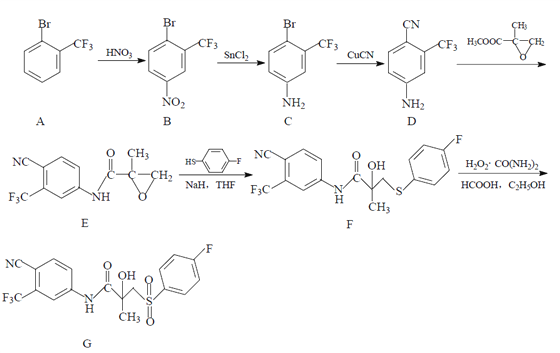
(1)B 中的含氧官能团名称为 _______________ ;
(2)C→D的反应类型为 __________________ ;
(3)写出同时满足下列条件的 D 的一种同分异构体的结构简式:_______________ ;
①有苯环;②能使溴的 CCl4 溶液褪色;③分子中有 2 种不同化学环境的氢
(4)合成 F 时还可能生成一种副产物 X,X 的结构简式为 _________________ ;
(5)已知 : 苯胺 (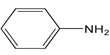 ) 易被氧化,请以甲苯和甲醇为原料制备
) 易被氧化,请以甲苯和甲醇为原料制备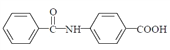 。________________
。________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空
(I)写出下列反应的热化学方程式。
(1)N2(气态)与H2(气态)起反应,完全反应生成34g NH3(气态)放出92.2 kJ的热量:________________________________________。
(2)标况下22.4L N2(气态)与适量O2(气态)起反应,生成NO(气态)需吸收68 kJ的热量:______________________________________。
(3)卫星发射时可用肼(N2H4)为燃料,1 mol N2H4(气态)在O2(气态)中燃烧,生成N2(气态)和H2O(气态),放出534 kJ的热量:__________________________________________。
(4)已知断裂1 mol H—H键、1 mol N≡N键分别需要吸收436 kJ、946 kJ的能量,生成1 mol N—H键放出391 kJ的能量,试写出N2(g)与H2(g)反应生成NH3(g)的热化学方程式:___________________________________。
(II)已知: C(s)+ O2(g) === CO2(g) ΔH=-393.5 kJ/mol
2CO(g)+O2(g) === 2CO2(g) ΔH=-566 kJ/mol
TiO2(s)+2Cl2(g) === TiCl4(s)+O2(g) ΔH=+141 kJ/mol
则TiO2(s)+2Cl2(g)+2C(s) === TiCl4(s)+2CO(g) ΔH= __________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学-选修3:物质结构与性质】磷是人体含量较多的元素之一,磷的化合物在药物生产和农药制造等方面用途非常广泛。回答下列问题:
(1)基态磷原子核外共有________个未成对的电子。
(2)P4S3可用于制造火柴,其结构如图所示。

①电负性:磷_______硫;第一电离能:磷_______硫; (填“>”或“<)。
②P4S3中硫原子的杂化轨道类型为_______。
(3)N、P、As、Sb均是第VA族的元素。
①上述元素的氢化物的沸点关系如图乙所示,沸点:PH33,原因是_______;沸点:PH333,原因是_______。
②某种磁性氮化铁的晶胞结构如图丙所示,该化合物的化学式为_______。
(4)磷化铝熔点为2000℃,它与晶体硅互为等电子体,磷化铝晶胞结构如图丁所示。
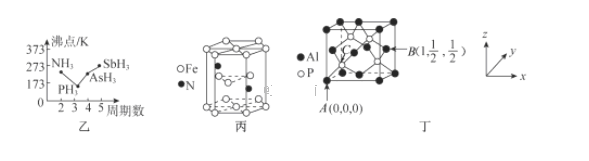
①图中A点和B点的原子坐标参数如图丁所示,则C点的原子坐标参数为_______。
②磷化铝晶体的密度为ρg·cm-3用NA表示阿伏加德罗常数的数值,则该晶胞中距离最近的两个铝原子之间的距离为_______cm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于同温同压下等体积的CO2和CO,下列叙述:①质量相等;②密度相等;③所含分子数相等;④所含碳原子数相等,其中正确的是( )
A.①②③④
B.②③④
C.③④
D.③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com