
 2NH3 (g) △H1
2NH3 (g) △H1 2NH3(g) △H=-92.4 kJ/mol
2NH3(g) △H=-92.4 kJ/mol| 容器编号 | 起始时各物质物质的量/mol | 平衡时反应 | ||
| N2 | H2 | NH3 | ||
| a | 1 | 3 | 0 | 23.1 |
| b | 2 | 6 | 0 | 未知(用E表示) |
 2NH3(g) △H<0 。
2NH3(g) △H<0 。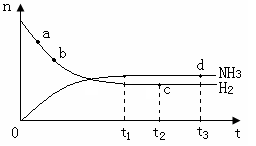
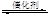 CH3OCH3(g)+3H2O(g) △H<0
CH3OCH3(g)+3H2O(g) △H<0| 容器 | c(CO2) /mol·L-1 | c(H2) /mol·L-1 | c(CH3OCH3) /mol·L-1 | c(H2O) /mol·L-1 | v (正)和v (逆)比较 |
| 容器I | 1.0×10-2 | 1.0×10-2 | 1.0×10-4 | 1.0×10-4 | v (正)=v (逆) |
| 容器II | 2.0×10-2 | 1.0×10-2 | 1.0×10-4 | 2.0×10-4 | |
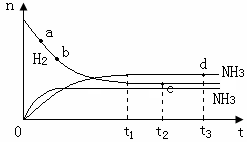 (2分)
(2分)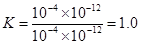 。根据表中数据可知
。根据表中数据可知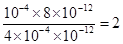 >1,所以正反应速率小于逆反应速率。
>1,所以正反应速率小于逆反应速率。

科目:高中化学 来源:不详 题型:填空题

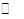 CO(g)+3H2(g) △H>0。
CO(g)+3H2(g) △H>0。 CH3OH(g),CO的平衡转化率与温度、压强的关系如右图所示,则:
CH3OH(g),CO的平衡转化率与温度、压强的关系如右图所示,则: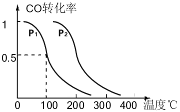
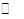 CH3OH(g)的平衡常数K的值为
CH3OH(g)的平衡常数K的值为 查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| t/min | X/mol | Y/mol | Z/mol |
| 0 | 1.00 | 2.00 | 0.00 |
| 1 | 0.90 | 1.80 | 0.20 |
| 3 | 0.75 | 1.50 | 0.50 |
| 5 | 0.65 | 1.30 | 0.70 |
| 9 | 0.55 | 1.10 | 0.90 |
| 10 | 0.55 | 1.10 | 0.90 |
| 14 | 0.55 | 1.10 | 0.90 |
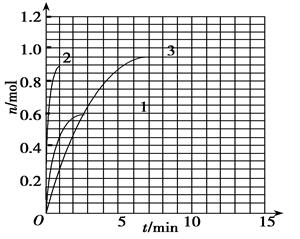
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 CoCl(aq) ΔH>0
CoCl(aq) ΔH>0| A.将盛有CoCl2和盐酸混合液的试管置于热水中,试管内溶液为红色 |
| B.升高温度,正反应速率增大,逆反应速率减小 |
| C.该反应的平衡常数K= |
| D.增大Cl-浓度,平衡向正反应方向移动,试管内溶液变为蓝色 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 C(g)+ D(g),能说明该反应达到平衡状态的标志是
C(g)+ D(g),能说明该反应达到平衡状态的标志是| A.平衡体系的总压不变 |
| B.平衡混合气体的平均相对分子质量不变 |
| C.C 和D的物质的量相等 |
| D.平衡混合气体的总物质的量不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
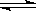 2Z(g)此反应达到平衡的标志是
2Z(g)此反应达到平衡的标志是 | A.容器内压强不随时间变化 |
| B.容器内各物质的浓度不随时间变化 |
| C.容器内X、Y、Z的浓度之比为1︰2︰2 |
| D.单位时间消耗0.1mol X同时生成0.2mol Z |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
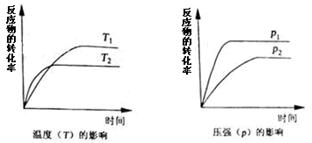
A.2NO2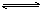 N2O4 (正反应放热) N2O4 (正反应放热) |
B.NH4HCO3(s) 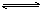 NH3+H2O (g)+CO2(正反应吸热) NH3+H2O (g)+CO2(正反应吸热) |
C.H2(g)+I2(g)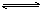 2HI(g) (正反应放热) 2HI(g) (正反应放热) |
D.3O2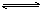 2O3(正反应为吸热反应) 2O3(正反应为吸热反应) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
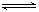 PCl3(g) + Cl2(g)。
PCl3(g) + Cl2(g)。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
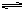 CO2(g)+H2(g),已知CO和H2O(g)的初始浓度为0.01mol·L-1时,H2平衡浓度为0.005mol·L-1。若此时再加入0.02mol·L-1的H2O(g),重新达到平衡时,H2平衡浓度为
CO2(g)+H2(g),已知CO和H2O(g)的初始浓度为0.01mol·L-1时,H2平衡浓度为0.005mol·L-1。若此时再加入0.02mol·L-1的H2O(g),重新达到平衡时,H2平衡浓度为 | A.0.0025 mol·L-1 | B.0.0075 mol·L-1 | C.0.010 mol·L-1 | D.0.015 mol·L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com