
【题目】某学生设计如图所示的实验装置,利用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应)。请回答下列问题:

(1)A为实验室制氯气的发生装置,反应化学方程式为_________________________;某学生用12 mol·L-1的浓盐酸100 mL和足量的MnO2反应制Cl2,实际得到的Cl2________6.72 L(填“<”、“>”或“=”)。
(2)漂白粉将在U形管中产生,其化学方程式是_________________________________。
(3)此实验所得漂白粉的有效成分偏低。该学生经分析并查阅资料发现,主要原因是在U形管中还存在两个副反应:
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是________________。
②Cl2中含HCl,会发生反应2HCl+Ca(OH)2===CaCl2+2H2O,为避免此副反应的发生,可将装置作何改进______________________________。
(4) C装置的作用是________________________________。
【答案】MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O < 2Cl2+2Ca(OH)2===CaCl2+Ca(ClO)2+2H2O 冷却B装置(或将B装置放在冷水浴中) 在A与B之间连接一个装有饱和氯化钠溶液的洗气瓶 吸收未反应完的氯气,防止污染空气
MnCl2+Cl2↑+2H2O < 2Cl2+2Ca(OH)2===CaCl2+Ca(ClO)2+2H2O 冷却B装置(或将B装置放在冷水浴中) 在A与B之间连接一个装有饱和氯化钠溶液的洗气瓶 吸收未反应完的氯气,防止污染空气
【解析】
装置A制备氯气,氯气在与消石灰发生反应得到次氯酸钙,氯气有毒,用碱液吸收。
(1)实验室制氯气的化学方程式为MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O;二氧化锰和稀盐酸不反应,随着反应的进行,盐酸浓度变稀,用12 mol·L-1的浓盐酸100 mL和足量的MnO2反应制Cl2,实际得到的Cl2<6.72 L;
MnCl2+Cl2↑+2H2O;二氧化锰和稀盐酸不反应,随着反应的进行,盐酸浓度变稀,用12 mol·L-1的浓盐酸100 mL和足量的MnO2反应制Cl2,实际得到的Cl2<6.72 L;
(2)氢氧化钙与氯气反应的化学方程式是2Cl2+2Ca(OH)2===CaCl2+Ca(ClO)2+2H2O;
(3)①氯气与氢氧化钙反应放热反应,温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是降低温度,将B装置放在冷水浴中;
②Cl2中含HCl,会发生反应2HCl+Ca(OH)2===CaCl2+2H2O,为避免此副反应的发生,先除去氯气中的氯化氢,可在A与B之间连接一个装有饱和氯化钠溶液的洗气瓶;
(4)氯气有毒,C装置的作用是吸收未反应完的氯气,防止污染空气。


科目:高中化学 来源: 题型:
【题目】TK时,向2.0 L恒容密闭容器中充入0.10 mol COCl2,发生反应COCl2(g)![]() Cl2(g)+CO(g),经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
Cl2(g)+CO(g),经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
t/s | 0 | 2 | 4 | 6 | 8 |
n(Cl2)/mol | 0 | 0.030 | 0.039 | 0.040 | 0.040 |
下列说法正确的是
A. 保持其他条件不变,升高温度,平衡时c(Cl2)=0.022 mol·L-1,则反应的ΔH<0
B. 反应在前2 s的平均速率v(CO)=0.015 mol·L-1·s-1
C. 保持其他条件不变,起始向容器中充入0.12 mol COCl2、0.06 mol Cl2和0.06 mol CO,反应达到平衡前的速率:v正<v逆
D. 保持其他条件不变,起始向容器中充入0.10 mol Cl2和0.08 mol CO,达到平衡时,Cl2的转化率小于60%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第4周期的A、B、C、D四种元素,其最外层电子数依次为1、2、2、7。其原子序数按A、B、C、D顺序增大,已知A和B的次外层电子数均为8,而C与D的次外层电子数均为18,根据结构用元素符号或化学式填空:
(1)写出元素名称:A____、B_____、C _____、D ____。
(2)D的简单离子的电子排布式_______________。
(3)元素的氢氧化物碱性最强的是______________。
(4)B原子与D原子间形成化合物的电子式为____________。
(5)写出A、B的第一电离能大小____________________。
(6)写出C基态原子的外围电子排布图______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是有机合成中的部分片段:
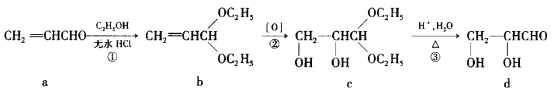
下列说法错误的是
A.有机物a能发生加成、氧化、取代等反应
B.有机物a~d都能使酸性高锰酸钾溶液褪色
C.d中所有原子不可能共平面
D.与b互为同分异构体、含有1个![]() 和2个
和2个![]() 的有机物有4种
的有机物有4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是一种微生物燃料电池的工作原理示意图,工作过程中必须对某室进行严格密封。下列有关说法错误的是
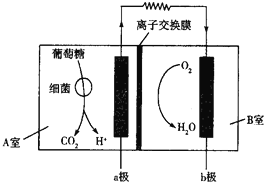
A.a极的电极反应式为![]()
B.若所用离子交换膜为质子交换膜,则![]() 将由A室移向B室
将由A室移向B室
C.根据图示,该电池也可以在碱性环境中工作
D.由于A室内存在细菌,所以对A室必须严格密封,以确保厌氧环境
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质由短周期原子序数依次增大的元素A、B、C、D、E构成,有如图所示关系:
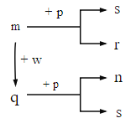
已知:①A的原子半径在周期表中最小。
②n由四种元素组成,既可用于厨房食品的膨松剂又可在医药方面用于治疗胃酸过多的患者。
③n、m、q、s四种物质焰色反应中火焰均为黄色。
④p由A、E的单质在光照或点燃的条件下化合得到
回答下列问题
(1)A元素为___(填名称,下同)、B元素为___、E元素为___。
(2)写出w的电子式___,且该化合物中化学键的类型___(填离子键、极性共价键或非极性共价键)。
(3)m溶液可以和p溶液反应生成r和s,写出该离子方程式___。
(4)q、r、w反应可以生成n,n的固体也可以在加热的条件下反应生成q、r、w,写出n的固体加热生成q、r、w的化学方程式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知烃A的分子式为C6H12,分子中含有碳碳双键,且仅有一种类型的氢原子,在下面的转化关系中,D1、D2互为同分异构体,E1、E2互为同分异构体。

(1)反应②的化学方程式为
___________________________________________________________;
(2)C的化学名称是_____________________________;E2的结构简式是_______________________;
(3)④、⑥的反应类型依次是_________________________、__________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物G是一种高分子化合物,常用作有机合成的中间体,并可用作乳胶漆等。可以通过以下途径合成:

已知有机物A中含有C、H、O、Cl四种元素且同一个碳原子上不直接连接两个官能团,E是乙醇的同系物,F的分子式为C4H6O2。
完成下列填空:
(1)A的结构简式为______或_________,反应③的反应类型________。
(2)写出反应⑤和反应⑥的化学方程式:
反应⑤___________________;反应⑥_____________。
(3)写出两种与F含有相同官能团的同分异构体的结构简式_______、_______。
(4)试设计一条以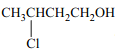 为原料合成
为原料合成![]() 的合成路线。(合成路线常用的表示方式为:
的合成路线。(合成路线常用的表示方式为:![]() )___________________
)___________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下式表示一种有机物的结构,关于它的性质的叙述中不正确的是
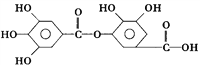
A. 它有酸性,能与Na2CO3溶液反应
B. 它可以水解,水解产物只有一种
C. 1mol该有机物最多能和8mol NaOH反应
D. 1mol该有机物最多能和8mol H2发生加成反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com