
 ”分别表示不同元素的原子.下列各项中对图示模型理解正确的是( )
”分别表示不同元素的原子.下列各项中对图示模型理解正确的是( )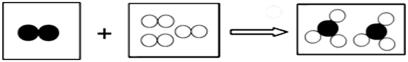
| A. | 该反应属于分解反应 | |
| B. | 反应中共有两种元素参与 | |
| C. | 反应物和生成物中只有一种单质 | |
| D. | 参加反应的两种物质分子个数之比为2:3 |
科目:高中化学 来源: 题型:实验题

 +Br2$\stackrel{催化剂}{→}$
+Br2$\stackrel{催化剂}{→}$ +HBr.
+HBr.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 高温、低压 | B. | 低温、高压 | C. | 低温、低压 | D. | 高温、高压 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H5Cl | B. | C2H4Cl2 | C. | C2H6 | D. | C2H5OH |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 利用电化学原理将CO、SO2转化为重要化工原料,装置如图所示:
利用电化学原理将CO、SO2转化为重要化工原料,装置如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
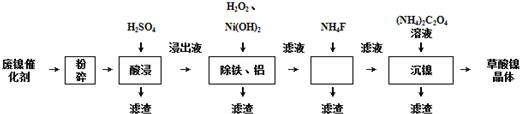
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Al3+ | 3.0 | 5.0 |
| Ni2+ | 6.7 | 9.5 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H+、Ca2+、Cl-、CO32- | B. | Na+、Mg2+、SO42-、OH- | ||
| C. | K+、Na+、Cl-、OH- | D. | Ba2+、Cu2+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 以石墨作电极电解饱和氯化钠溶液:2Cl-+2H2O$\stackrel{电解}{→}$ 2OH-+H2↑+Cl2↑ | |
| B. | Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+→Fe3++3H2O | |
| C. | H218O中投入少量Na2O2固体:2H218O+2O22-→4OH-+18O2↑ | |
| D. | CuCl2溶液中加入NaHS溶液:Cu2++HS-→CuS↓+H+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com