
| A. | 在电解制备磷酸亚铁锂的过程中,阳极的电极反应式为:Fe+H2PO4-+Li+-2e-═LiFePO4+2H+ | |
| B. | 放电过程中Li+向负极移动,充电过程中Li+向阴极移动 | |
| C. | 充电时,LiFePO4既发生氧化反应又发生还原反应 | |
| D. | 该锂电池放电时正极反应式为FePO4+Li++e-═LiFePO4 |
分析 A、铁棒为阳极,本身放电;
B、原电池中阳离子向正极移动,电解池中阳离子向阴极移动;
C、充电时,总的电极反应式为:LiFePO4═Li+FePO4,Fe的化合价升高,而锂的化合价降低;
D、正极发生还原反应;
解答 解:A、铁棒为阳极,本身放电,所以电极反应式为:Fe+H2PO4-+Li+-2e-═LiFePO4+2H+,故A正确;
B、原电池中阳离子向正极移动,电解池中阳离子向阴极移动,所以放电过程中Li+向正极移动,充电过程中Li+向阴极移动,故B错误;
C、充电时,总的电极反应式为:LiFePO4═Li+FePO4,Fe的化合价升高,而锂的化合价降低,所以LiFePO4既发生氧化反应又发生还原反应,故C正确;
D、正极发生还原反应,所以电极反应式为:FePO4+Li++e-═LiFePO4,故D正确;
故选B.
点评 本题考查了电解原理,选项C根据电极反应式中元素化合价变化确定反应的类型,题目难度不大.


 全能测控期末小状元系列答案
全能测控期末小状元系列答案 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案科目:高中化学 来源: 题型:解答题
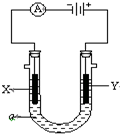 电解原理在化学工业中有广泛应用.
电解原理在化学工业中有广泛应用.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
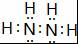 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑥ | B. | ②③④ | C. | ②③⑥ | D. | ④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6.4g 铜与S完全反应,电子转移0.1 NA个 | |
| B. | 标准状况下,2.24 L水中含有0.1 NA个水分子 | |
| C. | 1.12 L氯气中含有0.1 NA个氯原子 | |
| D. | 0.3molNO2与H2O反应转移的电子数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用与氢气的加成反应除去乙烷中的乙烯得到纯净的乙烷 | |
| B. | 利用溴水鉴别苯和甲苯 | |
| C. | 利用酸性高锰酸钾溶液鉴别乙苯和苯乙烯 | |
| D. | 利用四氯化碳萃取溴水中的溴 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com