
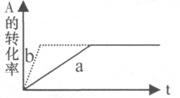
对于平衡体系mA(气)+nB(气) PC(气)十qD(气) △H <0,有下列判断,其中正确的是
 A.若温度不变,将容器的体积缩小1倍,此时A的浓度变为原来的1 .8倍,则m+n<p+q
A.若温度不变,将容器的体积缩小1倍,此时A的浓度变为原来的1 .8倍,则m+n<p+q
B.若平衡时,A、B的转化率相等,说明反应开始时A,B的物质的量之比为m:n
C.若平衡体系共有气体amol,再向其中加人bmolB,当重新达到平衡时,气体的总物质的量等于(a+b),则m+n>p+q
D.加催化剂或增大压强,可实现右图a→b的变化
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
城市使用的燃料,现大多用煤气、液化石油气。煤气的主要成分是CO和H2的混合气体,它由煤炭和水蒸气反应制得,故又称水煤气。
(1)试写出制取水煤气的主要化学方程式_______________________________。
(2)液化石油气的主要成分是丙烷,已知丙烷、CO以及氢气燃烧的热化学方程式分别为:
C3H8(g) +5O2(g) == 3CO2(g) + 4H2O(l) △H= –2220.0 kJ·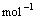
CO(g) +1/2O2(g) == CO2(g) △H= –282.6kJ·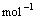
2H2(g)+O2(g) == 2H2O(l) △H= –571.6 kJ·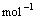
试比较同物质的量的C3H8和CO燃烧,产生的热量比值约为______________;
同质量的H2和C3H8燃烧,产生的热量比值约为________________。(计算结果保留小数点后一位数字)
(3)氢能源是21世纪极具开发前景的新能源之一,它既是绿色能源,又可循环使用。请在下图的两个空框中填上循环过程中的反应物和生成物,以完成理想的氢能源循环体系图(循环中接受太阳能的物质在自然界中广泛存在)。从能量转换的角度看,过程II主要是_______能转化为________能。
 |
查看答案和解析>>
科目:高中化学 来源: 题型:
有关碰撞理论,下列说法中不正确的是( )
A.具有足够能量的分子(活化分子)相互碰撞就一定能发生化学反应
B.增大反应物浓度,单位体积内活化分子数增多,有效碰撞的几率增大,反应速率增大
C.升高温度,活化分子百分数增大,有效碰撞的几率增大,反应速率增大
D.正催化剂能降低反应的活化能,提高活化分子百分数,有效碰撞的几率增大,反应速率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
在一固定容积的密闭容器中通入4molX气体和6molY气体,同时发生如下反应:X(气)+nY(气) 2R(气)+Q(气)反应达到平衡时,测得X和Y的转化率分别25%和50%,则n的值为( )
2R(气)+Q(气)反应达到平衡时,测得X和Y的转化率分别25%和50%,则n的值为( )
A、1 B、2 C、3 D、4
查看答案和解析>>
科目:高中化学 来源: 题型:
在10L容器中,加入2mol的SO2(g)和2mol的NO2(g),保持温度恒定,发生反应:
SO2(g)+ NO2(g) 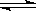 SO3(g)+NO(g)。当达到平衡状态时,测得容器中SO2(g)的转化率为50%。
SO3(g)+NO(g)。当达到平衡状态时,测得容器中SO2(g)的转化率为50%。
试求:该温度下、该容器中,再继续加入1mol的SO2(g),则:
(1)化学平衡将向________方向移动,NO2的转化率将____________;
(2)经计算,当达到新的平衡状态时,容器中SO2(g)的浓度是_______mol/L;
(3)整个过程中,SO2的转化率由50%变为_______%,NO2的转化率由__________%变为_______%。
(4)计算结果给我们的启示是:增大一种反应物物的用量,其转化率将________________(填“增大” 、“不变”或“减小”)另一反应物的转化率将____________(填“增大” 、“不变”或“减小”)。现实生产中的意义是:可以通过增大________的用量,来提高成本高的反应物的利用率。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列电离方程式中书写正确的是
A.NaHSO4  Na++H++SO42- B.NaHCO3
Na++H++SO42- B.NaHCO3  Na++H++CO32-
Na++H++CO32-
C.HClO = H++ClO- D.H2S  H++HS-;HS-
H++HS-;HS-  H++S2-
H++S2-
查看答案和解析>>
科目:高中化学 来源: 题型:
取c(H+)均为0.01 mol/L的盐酸和醋酸各100mL分别稀释2倍后,再分别加入0.03g锌粉,在相同条件下充分反应,有关叙述正确的是
① 醋酸与锌反应放出氢气多 ② 盐酸和醋酸分别与锌反应放出的氢气一样多
③ 盐酸与锌反应放出氢气多 ④ 盐酸和醋酸分别与锌反应的速度一样大
⑤ 醋酸与锌反应速率大 ⑥ 盐酸与锌反应速率大
A.①⑥ B.②⑤ C.③④ D.①⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
乙烯酮在一定条件下能与含活泼氢的化合物发生加成:

它与下列试剂发生加成反应时所生成的产物不正确的是
A.与HCl加成生成CH3COCl B.与H2O加成生成CH3COOH
C.与CH3OH加成生成CH3COCH2OH D.与CH3COOH加成生成(CH3CO)2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com