
| A.①③ | B.②③ | C.②④ | D.①② |
科目:高中化学 来源:不详 题型:填空题
| 成分 | NaCl | Mg(OH)2 | CaCO3 | BaSO4 | 其他不溶物 |
| 质量分数(%) | 15~20 | 15~20 | 5~10 | 30~40 | 10~15 |
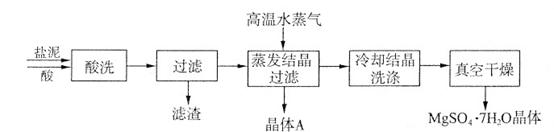
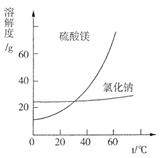
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
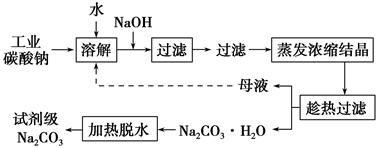
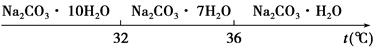
| 物质 | CaCO3 | MgCO3 | Ca(OH)2 | Mg(OH)2 | Fe(OH)3 |
| Ksp | 4.96×10-9 | 6.82×10-6 | 4.68×10-6 | 5.61×10-12 | 2.64×10-39 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氯碱工业是利用电解原理来生产氯气和纯碱 |
| B.农业生产中可将氮肥硫酸铵与钾肥碳酸钾混合使用 |
| C.区分食盐是否加碘的方法是观察食盐是否略显紫色 |
| D.可用点燃的方法鉴别衣物是否为丝织品、毛织品 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | 实验操作或事实 | 实验目的或结论 |
| A | 取少量试液于试管中,加入用HNO3酸化的BaCl2溶液,产生白色沉淀 | 说明试液中一定含有SO42- |
| B | 分别向两支试管中加入等体积、等浓度的过氧化氢溶液,再在其中一支试管中加入少量MnO2 | 研究催化剂对过氧化氢分解速率的影响 |
| C | 将NaHCO3与HCl两种溶液相互滴加 | 可以鉴别这两种溶液 |
| D | C2H5Br与AgNO3溶液混合加热 | 检验C2H5Br中的溴元素 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
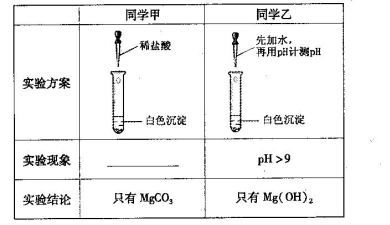
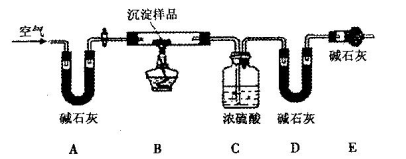
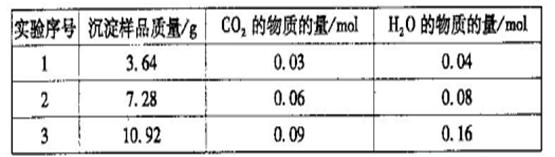
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
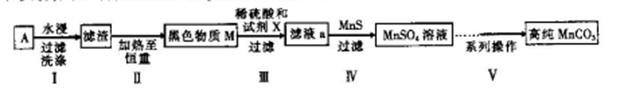

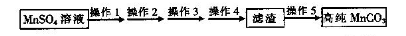
 已除干净; 操作4:___________________;
已除干净; 操作4:___________________; 查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题


| A.从KI和I2的固体混合物中回收I2,可使用如图甲所示实验装置 |
| B.分离Na2CO3溶液和CH3COOC2H5,可使用如图乙所示实验装置 |
| C.实验室制氨气,如图丙所示 |
| D.分离乙醇和乙酸的混合液,实验装置如图丁所示 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
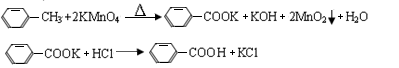
| 名称 | 相对分子质量 | 性状 | 熔点 | 沸点 | 密度 | 溶解度 | ||
| 水 | 乙醇 | 乙醚 | ||||||
| 甲苯 | 92 | 无色液体易燃易挥发 | -95 | 110.6 | 0.8669 | 不溶 | ∞ | ∞ |
| 苯甲酸 | 122 | 白色片状或针状晶体 | 122.4 | 248 | 1.2659 | 微溶 | 易溶 | 易溶 |

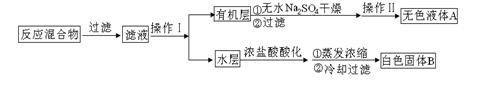
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com