


 £®
£® £®
£® £®
£®·ÖĪö øł¾ŻĢāÖŠø÷ĪļÖŹ×Ŗ»Æ¹ŲĻµ£¬½įŗĻĢāÖŠŠÅĻ¢æÉÖŖ£¬¼×±½ŌŚ¹āÕÕĢõ¼žĻĀÓėĀČĘų·“Ӧɜ³ÉAĪŖ £¬A·¢Éś¼īŠŌĖ®½āµĆBĪŖ
£¬A·¢Éś¼īŠŌĖ®½āµĆBĪŖ £¬B·¢ÉśŃõ»Æ·“Ó¦µĆCĪŖ
£¬B·¢ÉśŃõ»Æ·“Ó¦µĆCĪŖ £¬C·¢ÉśŠÅĻ¢ÖŠµÄ·“Ó¦µĆDĪŖ
£¬C·¢ÉśŠÅĻ¢ÖŠµÄ·“Ó¦µĆDĪŖ £¬DĖįŠŌĖ®½āµĆEĪŖ
£¬DĖįŠŌĖ®½āµĆEĪŖ £¬øł¾ŻFµÄ·Ö×ÓŹ½æÉÖŖ£¬ŅŅ“¼Ńõ»Æ³ÉŅŅĖį£¬ŅŅĖįŌŁÓėSOCl2·¢ÉśŠÅĻ¢ÖŠµÄ·“Ӧɜ³ÉFĪŖCH3COCl£¬FŗĶE·¢ÉśČ”“ś·“Ӧɜ³ÉGĪŖ
£¬øł¾ŻFµÄ·Ö×ÓŹ½æÉÖŖ£¬ŅŅ“¼Ńõ»Æ³ÉŅŅĖį£¬ŅŅĖįŌŁÓėSOCl2·¢ÉśŠÅĻ¢ÖŠµÄ·“Ӧɜ³ÉFĪŖCH3COCl£¬FŗĶE·¢ÉśČ”“ś·“Ӧɜ³ÉGĪŖ £¬GÓėSOCl2·“Ӧɜ³ÉŅŅõ£»ł±āĢŅõ£ĀČ£¬¾Ż“Ė“šĢā£®
£¬GÓėSOCl2·“Ӧɜ³ÉŅŅõ£»ł±āĢŅõ£ĀČ£¬¾Ż“Ė“šĢā£®
½ā“š ½ā£ŗøł¾ŻĢāÖŠø÷ĪļÖŹ×Ŗ»Æ¹ŲĻµ£¬½įŗĻĢāÖŠŠÅĻ¢æÉÖŖ£¬¼×±½ŌŚ¹āÕÕĢõ¼žĻĀÓėĀČĘų·“Ӧɜ³ÉAĪŖ £¬A·¢Éś¼īŠŌĖ®½āµĆBĪŖ
£¬A·¢Éś¼īŠŌĖ®½āµĆBĪŖ £¬B·¢ÉśŃõ»Æ·“Ó¦µĆCĪŖ
£¬B·¢ÉśŃõ»Æ·“Ó¦µĆCĪŖ £¬C·¢ÉśŠÅĻ¢ÖŠµÄ·“Ó¦µĆDĪŖ
£¬C·¢ÉśŠÅĻ¢ÖŠµÄ·“Ó¦µĆDĪŖ £¬DĖįŠŌĖ®½āµĆEĪŖ
£¬DĖįŠŌĖ®½āµĆEĪŖ £¬øł¾ŻFµÄ·Ö×ÓŹ½æÉÖŖ£¬ŅŅ“¼Ńõ»Æ³ÉŅŅĖį£¬ŅŅĖįŌŁÓėSOCl2·¢ÉśŠÅĻ¢ÖŠµÄ·“Ӧɜ³ÉFĪŖCH3COCl£¬FŗĶE·¢ÉśČ”“ś·“Ӧɜ³ÉGĪŖ
£¬øł¾ŻFµÄ·Ö×ÓŹ½æÉÖŖ£¬ŅŅ“¼Ńõ»Æ³ÉŅŅĖį£¬ŅŅĖįŌŁÓėSOCl2·¢ÉśŠÅĻ¢ÖŠµÄ·“Ӧɜ³ÉFĪŖCH3COCl£¬FŗĶE·¢ÉśČ”“ś·“Ӧɜ³ÉGĪŖ £¬GÓėSOCl2·“Ӧɜ³ÉŅŅõ£»ł±āĢŅõ£ĀČ£¬
£¬GÓėSOCl2·“Ӧɜ³ÉŅŅõ£»ł±āĢŅõ£ĀČ£¬
£Ø1£©øł¾ŻÉĻĆęµÄ·ÖĪöæÉÖŖ£¬DµÄ½į¹¹¼ņŹ½ ĪŖ £¬
£¬
¹Ź“š°øĪŖ£ŗ £»
£»
£Ø2£©A£®AĪŖ £¬
£¬ ÄÜ·¢ÉśČ”“ś·“Ó¦£¬¹ŹA“ķĪó£»
ÄÜ·¢ÉśČ”“ś·“Ó¦£¬¹ŹA“ķĪó£»
B£®BĪŖ £¬»ÆŗĻĪļB²»ÄÜ·¢ÉśŅų¾µ·“Ó¦£¬¹ŹB“ķĪó£»
£¬»ÆŗĻĪļB²»ÄÜ·¢ÉśŅų¾µ·“Ó¦£¬¹ŹB“ķĪó£»
C£®CĪŖ £¬»ÆŗĻĪļCÄÜ·¢ÉśŃõ»Æ·“Ó¦£¬¹ŹCÕżČ·£»
£¬»ÆŗĻĪļCÄÜ·¢ÉśŃõ»Æ·“Ó¦£¬¹ŹCÕżČ·£»
D£®“Ó¼×±½µ½»ÆŗĻĪļCµÄ×Ŗ»Æ¹ż³ĢÖŠ£¬Éę¼°µ½µÄ·“Ó¦ĄąŠĶÓŠČ”“ś·“Ó¦”¢Ė®½ā·“Ó¦ŗĶŃõ»Æ·“Ó¦£¬¹ŹD“ķĪó£¬
¹ŹŃ”C£»
£Ø3£©FŗĶE·¢ÉśČ”“ś·“Ӧɜ³ÉGĪŖ £¬ĖłŅŌE+F”śGµÄ»Æѧ·½³ĢŹ½ŹĒ
£¬ĖłŅŌE+F”śGµÄ»Æѧ·½³ĢŹ½ŹĒ £¬
£¬
¹Ź“š°øĪŖ£ŗ £»
£»
£Ø4£©DµÄ½į¹¹¼ņŹ½ ĪŖ £¬øł¾ŻĢõ¼ž£ŗ¢ŁŗģĶā¹āĘ×¼ģ²ā±ķĆ÷·Ö×ÓÖŠŗ¬ÓŠĒ軳£Ø-CN£©£»¢Ś1H-NMRĘ×¼ģ²ā±ķĆ÷·Ö×ÓÖŠÓŠ±½»·£¬ĒŅ±½»·ÉĻÓŠĮ½ÖÖ²»Ķ¬»Æѧ»·¾³µÄĒāŌ×Ó£¬¼“±½»·ÉĻÓŠĮ½øö“¦ÓŚ¶ŌĪ»µÄ»łĶÅ£¬Ōņ·ūŗĻĢõ¼žµÄDµÄ½į¹¹¼ņŹ½ĪŖ
£¬øł¾ŻĢõ¼ž£ŗ¢ŁŗģĶā¹āĘ×¼ģ²ā±ķĆ÷·Ö×ÓÖŠŗ¬ÓŠĒ軳£Ø-CN£©£»¢Ś1H-NMRĘ×¼ģ²ā±ķĆ÷·Ö×ÓÖŠÓŠ±½»·£¬ĒŅ±½»·ÉĻÓŠĮ½ÖÖ²»Ķ¬»Æѧ»·¾³µÄĒāŌ×Ó£¬¼“±½»·ÉĻÓŠĮ½øö“¦ÓŚ¶ŌĪ»µÄ»łĶÅ£¬Ōņ·ūŗĻĢõ¼žµÄDµÄ½į¹¹¼ņŹ½ĪŖ £¬
£¬
¹Ź“š°øĪŖ£ŗ £»
£»
£Ø5£©ŅŌŅŅ“¼ĪŖŌĮĻÖʱøF£¬æÉŅŌÓĆŅŅ“¼Ńõ»Æ³ÉŅŅĖį£¬ŅŅĖįŌŁÓėSOCl2·¢ÉśŠÅĻ¢ÖŠµÄ·“Ӧɜ³ÉFĪŖCH3COCl£¬·“Ó¦µÄŗĻ³ÉĀ·ĻßĪŖ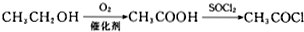 £¬
£¬
¹Ź“š°øĪŖ£ŗ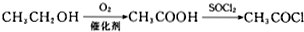 £®
£®
µćĘĄ ±¾ĢāÖ÷ŅŖæ¼²éµÄŹĒÓŠ»śĪļµÄŗĻ³ÉÓėÓŠ»śĪļµÄĶʶĻ£¬³ä·ÖÕĘĪÕ³£¼ūÓŠ»ś»ÆŗĻĪļµÄŠŌÖŹŅŌ¼°×„×”ĖłøųŠÅĻ¢½āĢāŹĒ¹Ų¼ü£¬ÄѶČÖŠµČ£¬×¢ŅāÓŠ»ś¹ŁÄÜĶŵĊŌÖŹµÄĮé»īŌĖÓĆ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 Č”ĪåøöĻąĶ¬µÄĘųĒņ£¬Ķ¬ĪĀĶ¬Ń¹ĻĀ£¬·Ö±š³äČėCOŗĶŅŌĻĀĖÄÖÖ»ģŗĻĘųĢ壬“µ³öĢå»żĻąµČµÄדæö£¬ČēĶ¼ĖłŹ¾£®A”¢B”¢C”¢DĖÄøöĘųĒņÄŚ£¬ÓėCOĖłŗ¬Ō×ÓŹżŅ»¶ØĻąµČµÄŹĒ£Ø””””£©
Č”ĪåøöĻąĶ¬µÄĘųĒņ£¬Ķ¬ĪĀĶ¬Ń¹ĻĀ£¬·Ö±š³äČėCOŗĶŅŌĻĀĖÄÖÖ»ģŗĻĘųĢ壬“µ³öĢå»żĻąµČµÄדæö£¬ČēĶ¼ĖłŹ¾£®A”¢B”¢C”¢DĖÄøöĘųĒņÄŚ£¬ÓėCOĖłŗ¬Ō×ÓŹżŅ»¶ØĻąµČµÄŹĒ£Ø””””£©| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | I-ŹĒøĆ·“Ó¦µÄ“߻ƼĮ | B£® | IO-Ņ²ŹĒøĆ·“Ó¦µÄ“߻ƼĮ | ||
| C£® | ·“Ó¦»ī»ÆÄܵČÓŚ98 kJ•mol-1 | D£® | v£ØH2O2£©=v£ØH2O£©=v£ØO2£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 Ņ»¶ØĪĀ¶ČĻĀ£¬ĻņČŻ»żĪŖ2LµÄĆܱÕČŻĘ÷ÖŠĶØČėĮ½ÖÖĘųĢ壬·¢Éś»Æѧ·“Ó¦£¬·“Ó¦ÖŠø÷ĪļÖŹµÄĪļÖŹµÄĮæ±ä»ÆČēĶ¼ĖłŹ¾£¬¶ŌøĆ·“Ó¦µÄĶʶĻ²»ŗĻĄķµÄŹĒ£Ø””””£©
Ņ»¶ØĪĀ¶ČĻĀ£¬ĻņČŻ»żĪŖ2LµÄĆܱÕČŻĘ÷ÖŠĶØČėĮ½ÖÖĘųĢ壬·¢Éś»Æѧ·“Ó¦£¬·“Ó¦ÖŠø÷ĪļÖŹµÄĪļÖŹµÄĮæ±ä»ÆČēĶ¼ĖłŹ¾£¬¶ŌøĆ·“Ó¦µÄĶʶĻ²»ŗĻĄķµÄŹĒ£Ø””””£©| A£® | øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ3B+4C?6A+2D | |
| B£® | ·“Ó¦½ųŠŠµ½1 sŹ±£¬v£ØA£©ŗĶv£ØD£©²»ĻąµČ | |
| C£® | ·“Ó¦½ųŠŠµ½6 sŹ±£¬BµÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ0.05 mol•L-1•s-1 | |
| D£® | ·“Ó¦½ųŠŠµ½6 sŹ±£¬ø÷ĪļÖŹµÄÅØ¶Č²»ŌŁ±ä»Æ£¬·“Ó¦ĖŁĀŹĪŖĮć |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CH4 £Øg£©+$\frac{3}{2}$O2£Øg£©ØT2H2O £Øl£©+CO £Øg£©”÷H1 | |
| B£® | S £Øs£©+$\frac{3}{2}$O2 £Øg£©ØTSO3 £Øs£©”÷H2 | |
| C£® | C6H12O6 £Øs£©+6O2 £Øg£©ØT6CO2 £Øg£©+6H2O £Øl£©”÷H3 | |
| D£® | 2CO £Øg£©+O2£Øg£©ØT2CO2 £Øg£©”÷H4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
| t”ę | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
| ĢåĻµ | c£ØSO2£© mol/L | c£ØO2£© mol/L | c£ØSO3£© mol/L | ÅضČÉĢ |
| £Ø1£© | 0.0600 | 0.400 | 2.000 | ²»Ģī |
| £Ø2£© | 0.0960 | 0.300 | 0.500 | ²»Ģī |
| £Ø3£© | 0.0862 | 0.263 | 1.020 | ²»Ģī |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĮņĖįĀĮČÜŅŗÓė¹żĮæBa£ØOH£©2ČÜŅŗ·“Ó¦2Al3++3SO42-+3Ba2++8OH-=3BaSO4”ż+2A1O2-+4H2O | |
| B£® | Ģ¼ĖįÄĘČÜŅŗÖŠµĪ¼ÓŃĪĖįÖĮĒ”ŗĆŅŖ³öĻÖĘųÅŻŹ±Ķ£Ö¹£ŗCO32-+2H+=CO2”ü+H2O | |
| C£® | ĖįŠŌøßĆĢĖį¼ŲČÜŅŗÓėH2O2ČÜŅŗ»ģŗĻ£ŗ2MnO4-+3H2O2+6H+=2Mn2++6H2O+402”ü | |
| D£® | ĀČĘųĶØČėŃĒĮņĖįÄĘČÜŅŗÖŠ£ŗ2Cl2+SO32-+H2O=2Cl-+SO2”ü+2HClO |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com