
【题目】锑(Sb)在自然界一般以硫化物的形式存在,我国锑的蕴藏量占世界第一。从硫化物中提取单质锑一般是先在高温下将硫化物转化为氧化物,再用碳还原:2Sb2S3+3O2+6Fe=Sb4O6+6FeS①;Sb4O6+6C=4Sb+6CO②。下列说法正确的是( )
A. 反应②说明高温下Sb还原性比C强
B. 反应①中每生成1 mol FeS时,共转移2mol电子
C. 每生成1 mol Sb时,反应①与反应②中还原剂的物质的量之比为4︰3
D. 反应①②中氧化剂分别是Sb2S3、Sb4O6
【答案】B
【解析】
![]() 中,Fe元素的化合价由0升高为+2,O元素的化合价由0降低为-2价; Sb4O6+6C=4Sb+6CO②中,C元素的化合价由0升高为+2,Sb元素的化合价由+3价降低为0。
中,Fe元素的化合价由0升高为+2,O元素的化合价由0降低为-2价; Sb4O6+6C=4Sb+6CO②中,C元素的化合价由0升高为+2,Sb元素的化合价由+3价降低为0。
A. 反应②中C为还原剂,还原剂的还原性大于还原产物的还原性,则说明高温下C的还原性比Sb强,故A错误;
B. 反应①中每生成3molFeS时,共转移![]() mol电子,则反应①中每生成1molFeS时,共转移电子的物质的量
mol电子,则反应①中每生成1molFeS时,共转移电子的物质的量![]() ,故B正确;
,故B正确;
C. C.生成![]() 时,反应②C是还原剂,需要
时,反应②C是还原剂,需要![]() ,需要
,需要![]() ,反应①中Fe是还原剂,生成
,反应①中Fe是还原剂,生成![]() ,需要
,需要![]() ,故反应①与反应②中还原剂的物质的量之比为
,故反应①与反应②中还原剂的物质的量之比为![]() ,所以每生成1molSb时,反应①与反应②中还原剂的物质的量之比为
,所以每生成1molSb时,反应①与反应②中还原剂的物质的量之比为![]() ,故C错误;
,故C错误;
D. 反应①中O元素的化合价降低,氧气为氧化剂,而反应②中Sb元素的化合价降低,氧化剂是![]() ,故D错误;
,故D错误;
故答案选B。


 黄冈创优卷系列答案
黄冈创优卷系列答案科目:高中化学 来源: 题型:
【题目】将饱和的Fe Cl3溶液逐滴滴入沸水中,液体变为红褐色 :
(1)写出反应的化学方程式_____。
(2)将其装入U形管内,用石墨棒做电极,接通直流电源,通电一段时间后发现阴极附近颜色_____,这表明__________,这种现象称为_____。
(3)向其中逐滴加入过量稀硫酸,现象是______;原因是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】萜品油烯(D)可用作香料的原料,它可由A合成得到如下所示,下列说法正确的是 ( )
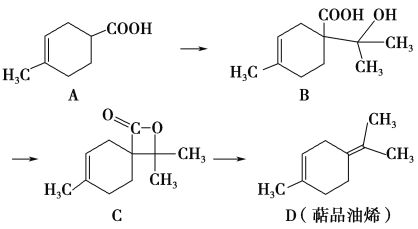
A. 有机物B的分子式为C11H19O3
B. 有机物D分子中所有碳原子一定共面
C. 1 mol有机物A中含有1.204×1024个双键
D. 有机物C的同分异构体中不可能有芳香化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香料M的一种合成流程如下:

已知:①![]()
②R1COOH![]() R1COOR
R1COOR
请回答下列问题:
(1)M中含碳的官能团名称是___________;设计R→X和Y→Z步骤的目的是___________。
(2)A→B的反应类型是___________,R分子中最多有___________个原子共平面。
(3)R和M在下列仪器中信号完全相同的是___________(填字母)
a红外光谱仪 b质谱仪 c元素分析仪 d核磁共振氢谱仪
(4)写出C和Z反应生成M的化学方程式:______________________。
(5)在Y的同分异构体中,同时满足下列条件的结构有___________种(不考虑立体异构)。
①能发生银镜反应
②遇氯化铁溶液发生显色反应
③1mol有机物最多能消耗3 mol NaOH
(6)已知苯环上有烃基时,新引入取代基主要取代邻位、对位氢原子。参照上述合成流程,设计以苯和异丙醇为原料制备Br![]() 的合成路线:_________________(无机试剂任选)
的合成路线:_________________(无机试剂任选)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)海水中蕴含的元素有80多种,它是一个巨大的宝藏。
①海水中被称为海洋元素是___。(填元素名称)
②下列物质不经过化学变化就能从海水中获得的是___。(填字母)
A.单质钠 B.单质碘 C.氯化钠
③加碘食盐中碘酸钾的化学式是___。
(2)实验室可以用高锰酸钾和浓盐酸反应制取氯气,反应的化学方程式如下:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
①在该反应的化学方程式上用双线桥标出电子转移的方向和数目___。
②该反应中浓盐酸表现的性质有___。
③如反应中转移了20mol电子,则产生的Cl2在标准状况下体积为__ L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种芳香族化合物都是某些植物挥发油中主要成分,有的是药物,有的是香料。它们的结构简式如下所示:
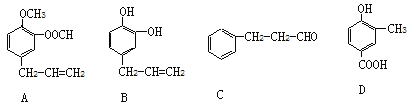
(1)写出上述有机物A中官能团的名称_______________________________________。
(2)能与新制Cu(OH)2反应的有________________________(用A、B、C、D填写)。写出含碳原子数较少的物质与新制Cu(OH)2反应生成砖红色沉淀的化学反应方程式:________________________________
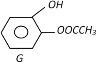
(3)① D一种同分异构体G的结构简式如上图:写出G与足量NaOH溶液共热反应方程式:_____________
② D的另一种同分异构体H,其苯环上有两个相邻的取代基,它既能使FeCl3溶液变紫色,又能与NaHCO3溶液反应放出CO2气体,H的结构简式是______________________________。
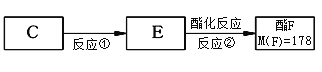
(4)按上图,C经一步反应可生成E,E是B的同分异构体,则反应①属于__________反应,F结构简式_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数,下列叙述正确的是( )
A. 64 g SO2含有氧原子数为1NA
B. 物质的量浓度为0.5 mol·L-1的MgCl2溶液,含有Cl-数为1 NA
C. 标准状况下,22.4 L H2O的分子数为1NA
D. 常温常压下,14 g N2含有分子数为0.5 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应mX(g)![]() nY(g)+pZ(g) ΔH,在不同温度下的平衡体系中物质Y的体积分数随压强变化的曲线如图所示,下列说法错误的是( )
nY(g)+pZ(g) ΔH,在不同温度下的平衡体系中物质Y的体积分数随压强变化的曲线如图所示,下列说法错误的是( )

A. 该反应的ΔH>0
B. m<n+p
C. B、C两点化学平衡常数:KB>KC
D. A、C两点的反应速率v(A)<v(C)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
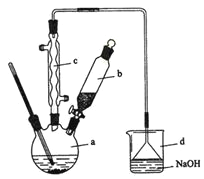
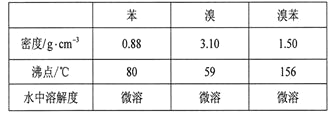
按下列合成步骤回答问题:
(1)在a中加入15 mL无水苯和少量铁屑。在b中小心加入4.0 mL液态溴。向a中滴入几滴溴,有白色烟雾产生,是因为生成了__________气体。继续滴加至液溴滴完。装置d的作用是__________________________________________;
(2)该反应的化学方程式:__________________________________________。
(3)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10 mL水,然后过滤除去未反应的铁屑;
②滤液依次用l0 mL水、8 mL l0%的NaOH溶液、10 mL水洗涤。NaOH溶液洗涤的作用是除去HBr和未反应的Br2;
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入氯化钙的目的是__________________________;
(4)经以上分离操作后,粗溴苯中还含有的主要杂质为_______,要进一步提纯,下列操作中必须的是______(填入正确选项前的字母);
A重结晶 B过滤 C蒸馏 D萃取
(5)在该实验中,a的容积最适合的是______(填入正确选项前的字母)。
A.25 mL B .50 mL C. 250 mL D. 509 mL
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com